5월 허가 의약품 총 190개…전문약은 157개
당뇨약, 고혈압-고지혈증 4제 복합제, 장티푸스 백신 등 다양한 품목들 허가
- 노영희 기자 nyh2152@medifonews.com
- 등록 2022-06-04 05:55:50
2022년 5월 190개의 의약품이 식약처로부터 허가를 받았다. 지난 4월 대비 허가된 의약품 수는 적지만 일반의약품 대비 전문의약품의 허가 비중은 5월이 더 높았다.
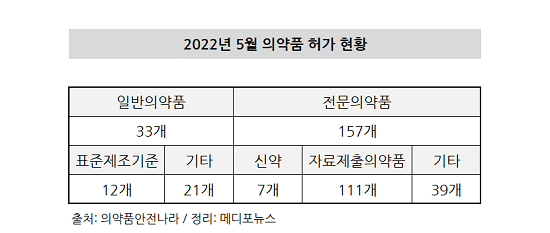
허가된 190개의 의약품 중 일반의약품은 33품목, 전문의약품은 157품목이었다.
일반의약품 33개 중 표준제조기준은 12품목, 기타는 21품목 해당됐으며 전문의약품 157개 중에서는 신약 7품목, 자료제출의약품 111품목, 기타 39품목 해당됐다.
전문의약품 중에서는 녹십자가 10건으로 가장 많은 품목을 허가받았다. 세부적으로 살펴보면 시타네오듀오, 네오다파, 로제텔핀 등 3가지 제품에 대한 다른 용량들이 허가받았다.
시타네오듀오서방정은 100/1000mg, 50/1000mg, 50/500mg에 대해 허가받은 시타글립틴 성분의 당뇨약이다.
네오다파정은 10mg에 대해 허가받았으며 세부 정보는 확인되지 않았지만 다파글리플로진 성분의 약제인 것으로 보아 당뇨약으로 추정된다.
로제텔핀정은 80/20/10/5mg, 40/5/10/5mg, 80/5/10/5mg, 80/10/10/5mg, 40/10/10/5mg, 40/20/10/5mg 여섯개 용량에 대해 허가받았다.
로제텔핀은 고혈압과 이상지질혈증에 대한 4제 복합제다. 고혈압 치료 성분인 텔미사르탄, 암로디핀과 이상지질혈증 치료 성분인 로수바스타틴, 에제티미브 성분이 포함됐다.
녹십자에 따르면 로제텔핀은 고혈압과 고지혈증을 동반한 국내 환자 약 130명을 대상으로 진행한 임상 3상에서 유효성을 확인했다. 임상 결과, ‘로제텔핀’은 대조군 대비 혈관 수축기 혈압(msSBP) 변화량과 저밀도 지단백 콜레스테롤(LDL-C) 변화율에서 효과가 있음을 입증했다.
녹십자 외에도 노보노디스크, SK바이오사이언스, 바이엘, BMS 등 많은 제약∙바이오사에서 품목허가 소식을 알렸다.
노보노디스크는 당뇨약은 리벨서스와 오젬픽에 대해서 허가를 받았다.
두 제품 모두 세마글루티드 성분의 당뇨약이지만 리벨서스는 GLP-1 유사체 경구용 2형당뇨병 치료제, 오젬픽 프리필드펜은 주1회 투여 2형당뇨병이라는 점에서 다소 차이가 있다.
리벨서스는 임상시험인 PIONEER 연구를 통해 DPP-4 억제제와 SGLT-2 억제제 대비 우월한 혈당 강하 효과는 물론 부수적으로 체중 조절의 이점이 확인됐다.
오젬픽은 주 1회 투여 주사제로, 2형당뇨병과 확증된 심혈관계 질환 성인 환자에서 주요 심혈관계 사건 위험성을 감소시키기 위해 투여할 수 있도록 국내에서 관련 적응증을 가진 유일한 GLP-1 유사체 제제다.
SK바이오사이언스는 국제백신연구소와 공동 개발한 장티푸스백신 ‘스카이타이포이드 멀티주’의 수출용 품목허가를 획득했다.
스카이타이포이드는 1회 접종으로도 우수한 면역원성과 장기적 예방 효과를 기대할 수 있을 것으로 예상되고 있으며 생후 6개월~만 2세의 영유아에서도 접종 가능하다.
네팔에서 6개월 이상 만 45세 미만 2160명을 대상으로 진행한 임상 3상에서 우수한 면역원성과 안전성을 확인했으며, 이 연구 결과는 작년 12월 의학학술지 ‘란셋 감염병 저널’에 게재되며 공인받았다.
올해 1월에는 국제학술지 NPJ에 게재된 부스터샷 임상2상 결과에서는 생후 6~23개월 영유아를 대상으로 스카이타이포이드를 2회 접종할 경우, 접종 전보다 체내 항체가가 약 64배로 증가하는 등 강력한 면역 반응이 유도되는 것을 확인하기도 했다.
바이엘은 2형당뇨를 동반한 신장질환 치료제 ‘케렌디아’에 대해 허가를 받았다. 케렌디아는 2형당뇨가 있는 만성 신장병 성인 환자에서 추정 사구체 여과율의 지속적인 감소, 말기 신장병에 도달, 심혈관계 질환으로 인한 사망, 비치명적 심근경색 및 심부전으로 인한 입원의 위험 감소를 위해 승인됐다.
케렌디아는 최초의 무기질 코르티코이드 수용체의 비스테로이드성 선택적 길항제다. 케렌디아는 무기질코르티코이드 수용체 과활성화를 억제해 염증과 섬유화를 줄이고 신장 손상을 억제한다.
위약군과 비교연구한 FIDELIO-DKD 3상연구를 통해 케렌디아는 1차 복합 평가 변수인 말기신장병, 추정 사구체여과율의 40% 이상 지속적 감소, 신장 원인으로 인한 사망을 위약 대비 약 18% 유의하게 감소시켰으며 2차 평가 변수인 심혈관계 원인으로 인한 사망, 비치명적 심근경색, 비치명적 뇌졸중 또는 심부전으로 인한 입원도 약 14% 감소시켰다.
한편 일반의약품 중에서는 한올바이오파마의 ‘베로논디’, 안국약품의 ‘소피림 점안액’, 현대약품 ‘디나펜카타플라스마’, 일양약품 ‘비파인정’, 환인제약 ‘위아제정’ 등이 허가를 받았다.
관련기사
- 2026년 첫 달, 전문의약품 허가 60건…약 59.4% 2026-02-04
- 11월 의약품 허가 125건…전문의약품 57.6% 2025-12-03
- 10월 의약품 품목허가 86건…전문의약품 56.9% 2025-11-05
- 9월 의약품 품목허가 117건…전문의약품 71.7% 2025-10-11
- 8월 의약품 허가 91건…전문의약품 허가건수 과반 2025-09-04
- 7월 의약품 허가 중 67%는 전문의약품…희귀 1건 2025-08-01
- 6월 의약품 허가 92건 중 전문약 57.6%…희귀·항암제 두각 2025-07-02
- 4월 의약품 품목 허가, 전문의약품이 절반 2025-05-01
- 2월 의약품 74건 허가…전문의약품 66.2% 2025-03-05
- 1월 의약품 허가 58건 중 전문의약품은 34건 2025-02-05
- 전문약 허가 60%…2025년 치료현장 변화 기대 2025-01-06
- 11월 의약품 107건 허가…전문의약품 44.8% 2024-12-03
- 10월 의약품 허가 저조…전문의약품 30% 내외 2024-10-31
- 9월 품목허가 의약품 86개…전문의약품 40% 2024-10-02
- 8월 의약품 품목허가 48건…희귀질환 치료제 多 2024-09-02
- 7월 전문의약품 46개 허가…탈모약‧무좀약 多 2024-08-06
- 6월, ETC 허가 비중 낮지만 희귀의약품 허가 다수 확인 2024-07-02
- 2024년 5월 의약품 품목허가, 일반약>전문약 2024-06-04
- 4월 의약품 117건 허가…전문의약품 52% 2024-05-02
- 3월 허가 의약품 135건…전문의약품 66% 2024-04-03
- 2월 91개 의약품 허가…전문의약품 비중 59% 2024-03-04
- 1월 허가의약품, 일반약이 전문약 앞질러…총 86건 허가 2024-02-05
- 12월 총 64개 의약품 허가…59.3%는 전문의약품 2024-01-06
- 11월 조현병‧폐암 치료제 등 전문약 허가 비중 50% 2023-12-04
- 10월 의약품 품목허가 70건…적응증 다양화 2023-11-02
- 9월 품목허가 131건 중 전문의약품이 70% 2023-10-05
- 8월 허가 의약품, 전문의약품 74% 이상 차지 2023-09-04
- 7월 품목허가 저조…전문의약품 비중 30% 2023-08-01
- 5월 의약품 품목허가, 전문의약품 비중 69.3% 2023-06-02
- 4월 품목허가 건수, 일반의약품이 전문의약품 앞질러 2023-05-02
- 3월 허가된 의약품은 총 128건…전문의약품 68.7% 2023-04-05
- 2월 허가된 전문의약품 76개…전체의 75%↑ 2023-03-03
- 2023년 첫 달 허가 품목은 총 249개…전문약 86% 2023-02-06
- 12월 전문의약품 허가 비중은 전체 중 73%…103개 허가 2023-01-06
- 11월 허가된 의약품 112개 중 60%는 전문의약품 2022-12-03
- 10월 허가 의약품, 최저 수량에도 알짜배기 제품 다수 2022-11-01
- 9월 허가 의약품, 전문의약품 비중이 63% 이상 차지 2022-10-01
- 8월 의약품 품목허가 57건에 그쳐…전문약 30개 2022-09-01
- 7월 허가 의약품 119 품목 中 전문약은 88 품목 2022-08-08
- 6월 허가된 제품 97건 중 전문의약품은 74건 2022-07-04
- 4월 의약품 235개 허가…당뇨약 다수 2022-05-02
- 3월 의약품 허가 98개 허가…전문약 62개 2022-04-02
- 2월 의약품 108품목 허가…전문약 69개 2022-03-04
- 임인년 첫 달, 의약품 198개 품목허가 2022-02-04
- 식약청, 전문약 61개 등 품목허가 현황 발표 2010-01-22
- 식약청, ‘조페닐정’ 등 240품목 주간 허가 2010-01-08
- 식약청, '씨랜스정' 주간 의약품 품목취하 2009-12-18
- 주간 품목허가 현황, 스트라테라캡슐 등 총 53품목 2009-12-04
- 식약청, 지난주 품목허가(신고) 현황 총 23품목 2009-11-28
- 신종플루백신 등 주간의약품 56품목 허가 2009-10-30
- 녹십자 인플루엔자백신 등 허가 2009-07-31
- 개량신약인정 채택후 ‘아모잘탄정’ 등 첫 허가 2009-04-11
- ‘유리토스정’-‘두창백신’ 신약 등 신규 허가 2009-01-12
- [인사]경희대한방병원 이재동 교수, 대한한의학회 제40대 회장 취임
- [인사]라이트재단, 이민원 신임 대표이사 취임
- [인사]신장학회 박형천 이사장, 아시아-태평양신장학회 이사장 취임
- [동정]부산대병원 목정하 교수, ‵결핵예방의 날‵ 대통령 표창 수상
- [인사]제일파마홀딩스 임원 인사 및 조직개편
- [동정]순천향대 부천병원 이영구 교수, 대한스포츠의학회 ‘제마스포츠의학상’ 수상
- [동정]길병원 이시훈 교수, AOCE 2026 최우수 연제상 수상
- [인사]코오롱생명과학, 이한국 신임 대표이사 선임 (3/26)
- [인사]연세대학교 의료원 인사
- [동정]고대 안암병원 조경희 교수,서울시의회의장 표창 수상
- [인사]경희대한방병원 이재동 교수, 대한한의학회 제40대 회장 취임
- [인사]라이트재단, 이민원 신임 대표이사 취임
- [인사]신장학회 박형천 이사장, 아시아-태평양신장학회 이사장 취임
- [인사]제일파마홀딩스 임원 인사 및 조직개편
- [인사]코오롱생명과학, 이한국 신임 대표이사 선임 (3/26)
- [인사]연세대학교 의료원 인사
- [인사]분당제생병원 배종옥 간호부장, 제19대 성남시 간호사회 회장 취임
- [인사]경북대병원 박재찬 교수, 대한뇌혈관외과학회 회장 선출
- [인사]정영훈 前 복지부 한의약정책관, 진흥원 신임 기획이사 임명
- [인사]한국팜비오, 임원승진 인사 단행
- [동정]부산대병원 목정하 교수, ‵결핵예방의 날‵ 대통령 표창 수상
- [동정]순천향대 부천병원 이영구 교수, 대한스포츠의학회 ‘제마스포츠의학상’ 수상
- [동정]길병원 이시훈 교수, AOCE 2026 최우수 연제상 수상
- [동정]고대 안암병원 조경희 교수,서울시의회의장 표창 수상
- [동정]한미약품-한국여자醫, ‘젊은의학자학술상’에 이선영 부교수 선정
- [동정]고대 안산병원 박형준 교수, 대한연골 및 골관절염학회 학술대회 ‘우수연제’ 선정
- [동정]인천 남동구에 ‘가천이길여길’ 명예도로명 부여
- [동정]전남대병원 주성필 교수, 대한뇌혈관외과학회 ‘남천학술상’ 수상
- [동정]동국제약 판시딜·마데카솔, 2026년 한국산업의 브랜드파워조사 1위 선정
- [동정]강동경희대학교병원 박성혁 교수, ‘제5회 SP 자랑스런 병원인상’ 서울특별시장 표창 수상













