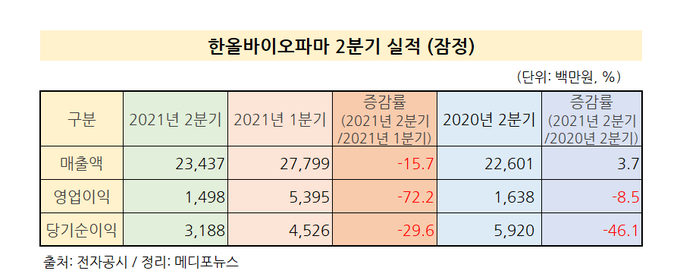
한올바이오파마는 28일 잠정 실적공시를 통해 2021년 2분기 연결 기준 매출액 234억원, 영업이익 16억원, 당기순이익 33억원을 달성했다고 밝혔다.
올해 상반기 누적 매출액은 512억원으로 작년 대비 15% 성장했고, 영업이익은 70억원으로 56% 증가했다. 특히 소화기 전문 항생제인 노르믹스와 전립선암 치료제 엘리가드, 프로바이오틱스 제품인 바이오탑 등 주력제품의 매출이 큰 폭으로 증가하면서 영업이익률도 14%로 작년 상반기 대비 4%p 높아졌다.
한올바이오파마는 상반기 말 기준 자산 2,038억원, 자본 1,625억원, 부채 413억원으로 부채비율 25%의 안정적인 재무구조를 유지하고 있다.
신약 파이프라인 중 ‘HL161(자가면역질환 치료 항체)’은 병원성 자가항체에 의해 발생하는 희귀 자가면역질환 치료 항체신약인 HL161(물질명: 바토클리맙, Batoclimab)이다. 현재 글로벌 라이선스 파트너인 이뮤노반트(Immunovant)와 하버바이오메드(Harbour Biomed)를 통해 미국과 중국에서 각각 개발 중이다.
미국에서 HL161의 임상개발을 진행하고 있는 이뮤노반트는 올해 초 콜레스테롤 증가 이슈로 일시 중지했던 임상시험의 재개 계획을 지난 6월 발표했다.
임상 참여 환자에 대한 종합적인 분석 결과, 콜레스테롤(LDL) 수치를 환자 모니터링과 투약 방법 및 주기 변경, 필요 시 콜레스테롤 조절 약물의 개인별 처방 등을 통해 안전하게 관리할 수 있다는 판단에 따른 것이다.
이뮤노반트는 준비 과정을 거쳐 올해 말 또는 내년 초에 중증 근무력증 임상3상, 갑상선 안병증 임상2상, 용혈성빈혈 임상2상 시험을 재개할 계획이며, 내년 상반기에 두 개의 추가 적응증에서의 임상을 시작할 계획이다.
한올바이오파마는 일본에서 중증 근무력증 환자 대상으로 임상3상을 준비하고 있고 이뮤노반트와 협업해 내년 중 임상을 시작할 예정이다. 다른 적응증에 대한 일본 임상도 계획하고 있으며, 순차적으로 진행해 나갈 예정이다.
중국에서는 하버바이오메드가 중증 근무력증과 혈소판 감소증, 시신경 척수염에 대한 HL161 임상2상 시험을 진행 중이다.
하버바이오메드는 지난 7월 중증 근무력증 임상2상 탑라인(topline) 결과를 발표했다.
임상시험 결과 주평가변수(primary endpoint)인 중증근무력증 환자의 일상생활수행능력(MG-ADL)에서 위약 대비 통계적으로 유의성 있는 개선(p=0.043)을 보였다. 함께 측정한 부평가변수(secondary endpoint)인 QMG, MGC, MG-QoL 등의 지표에서도 HL161은 투약 후 빠르게 증상 개선을 나타냈다.
HL161은 뛰어난 안전성과 내약성을 보였고, 심각한 이상반응(serious adverse events)이나 이상반응으로 인한 임상 이탈 환자도 없었다고 밝혔다. 하버바이오메드는 올해 하반기에 중증 근무력증 임상 3상에 진입한다는 계획이다.
한올바이오파마가 대웅제약과 공동 개발하고 있는 HL036 점안액(물질명: 탄파너셉트, Tanfanercept)는 안구내 염증을 유발하는 종양괴사인자(TNF)를 억제해 염증성 안구질환을 치료하기 위해 개발 중인 바이오 신약이다.
미국의 안구건조증 시장 공략을 위해 미국 현지에서 임상시험을 진행 중이며, 작년 상반기에 임상3-1상(VELOS-2 study)을 마쳤다.
한올바이오파마는 지난 7월 22일에 임상3-2상(VELOS-3 study) 시험계획서(IND)를 美 FDA에 제출했으며, 올해 3분기내에 임상을 시작해 내년 상반기에 탑라인(Topline) 결과를 확인할 수 있을 것으로 예상된다.
중국에서는 한올로부터 중국 지역에 대한 라이선스를 부여 받은 하버바이오메드가 중국 품목허가를 위한 임상3상 시험을 진행하고 있다. 지난 3월에 첫 환자 투약이 시작됐으며, 총 674명의 안구건조증 환자를 대상으로 HL036의 효능과 안전성을 평가할 예정이다.
한올바이오파마에서는 안구건조증 치료제로 임상3상 중인 HL036의 신규 적응증 확대를 위해 포도막염 등 다양한 염증성 안구질환에 적용하기 위한 연구를 하고 있다. 하반기에 신규 적응증과 임상전략을 확정할 계획이다.
이와 함께 대웅제약과 공동으로 TIGIT과 TIM-3를 타깃으로 하는 신규 면역항암항체 프로젝트‘
HL186/HL187 (면역항암 항체신약)’를 진행하고 있으며, 현재 동물모델에서 항암효과를 확인했고, IND를 제출하기 위한 전임상 시험을 준비 중에 있다.
관련기사
- 상위제약사 상반기 수출액은 8101억원…매출의 8.6% 2021-09-02
- 상위제약사, 영업활동 현금흐름 작년과 유사…5441억원 2021-08-27
- 직원들의 근속년수가 가장 긴 제약사는? 2021-08-26
- 상위 국내제약사, 1인당 매출 2억 3840만원 달성 2021-08-25
- 녹십자, 올 상반기 R&D 정부보조금 최다 수령…83억원 2021-08-24
- 상반기 상위제약사 접대비 비중 높아…대한뉴팜 최다 2021-08-23
- 제약사 상반기 ‘판촉비’, 작년 동기대비 10.3% 증가 2021-08-20
- 상반기 TOP50 제약사 판매관리비 매출대비 30.2% 지출 2021-08-20
- 상위 제약사, 상반기 연구개발비 작년 대비 46.6% 투자 2021-08-19
- 상위 50개 국내 제약사, 올해 상반기 매출 5.3% 성장 2021-08-18
- 종근당 그룹, 2분기 매출 연이은 고공행진 2021-08-17
- 휴젤, 상반기 매출 1284억원…글로벌 시장 확대 ‘훈풍’ 2021-08-11
- 한미약품, 코로나19 뚫고 2분기 호실적 달성 성공 2021-07-29
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [동정]가정의학과의사회 유승호 공보이사, 보건복지부 장관상 수상
- [동정]경북대병원 김혜정 연구교수·박준석 교수 연구팀, 대한대장항문학회 ‘우수포스터상’ 수상
- [동정]길병원 노영 교수, 치매 연구 공로, 보건의 날 맞아 복지부 장관 표창
- [동정]순천향대 부천병원 당뇨발 연구소, 서울국제창상학회 ‘최우수 구연상’ 수상
- [동정]경희대병원 유지욱 교수, 대한뇌혈관외과학회 최우수 학술상 수상
- [동정]고대 안암병원 김창곤 교수, 대한혈액학회 국제학술대회 최우수 포스터상 수상
- [인사]순천향대 부천병원 문종호 교수, ‘제19대 대한췌장담도학회 이사장’ 취임
- [인사]SK바이오, R&D 실행력 강화 위해 연구지원조직 정비 및 핵심인재 영입
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]순천향대 부천병원 문종호 교수, ‘제19대 대한췌장담도학회 이사장’ 취임
- [인사]SK바이오, R&D 실행력 강화 위해 연구지원조직 정비 및 핵심인재 영입
- [인사]화순전남대병원 김인영 교수, 대한정위기능신경외과학회장 선임
- [인사]원광대병원 김정우 교수, 대한견주관절학회 제34대 회장 취임
- [인사]일동제약그룹 정기승진인사 (4/1)
- [인사]한국산텐제약, 신임 대표이사에 김진희 대표 선임 (4/1)
- [인사]일동제약, 새 R&D 본부장 박재홍 사장 선임
- [인사]고대 안암병원 진윤태 교수, 대한소화기암연구학회 신임 이사장 취임
- [인사]연세대학교 의료원 인사(4/1)
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [동정]가정의학과의사회 유승호 공보이사, 보건복지부 장관상 수상
- [동정]경북대병원 김혜정 연구교수·박준석 교수 연구팀, 대한대장항문학회 ‘우수포스터상’ 수상
- [동정]길병원 노영 교수, 치매 연구 공로, 보건의 날 맞아 복지부 장관 표창
- [동정]순천향대 부천병원 당뇨발 연구소, 서울국제창상학회 ‘최우수 구연상’ 수상
- [동정]경희대병원 유지욱 교수, 대한뇌혈관외과학회 최우수 학술상 수상
- [동정]고대 안암병원 김창곤 교수, 대한혈액학회 국제학술대회 최우수 포스터상 수상
- [동정]울산대학교병원 박정익 교수, ‘두산연강 간담췌외과학술상’수상
- [동정]전북대병원 오영민 교수, 대한노인신경외과학회 ‘학술상’ 수상
- [동정]고대 안암병원 박민구 교수, 제43차 대한남성과학회 해외학술상 수상













