심장 재생과 기능 회복 조절하는 유전자 발견
유전자 ‘Cbx7’, 심근세포 증식과 심장 재생 능력 조절
심근세포 활성 감소 메커니즘 활용한 심부전 치료제 개발 기대
- 이형규 기자 kyu7179@medifonews.com
- 등록 2023-05-23 09:30:49
 심근세포의 증식과 심장의 재생능력을 조절하는 인자가 규명됐다.
심근세포의 증식과 심장의 재생능력을 조절하는 인자가 규명됐다.연세대학교 의과대학 의생명과학부 윤영섭 교수 연구팀은 심장의 재생과 기능적 회복에 중요한 역할을 하는 Cbx7 유전자를 발견하고, 마우스모델에서 Cbx7 유전자 활성 정도에 따른 심장 재생 효과를 규명했다고 23일 밝혔다. 이번 연구결과는 국제학술지 ‘서큘레이션’(Circulation, IF 39.92)에 게재됐다.
2019년 세계보건기구(WHO) 조사 결과에 따르면, 심혈관질환은 전 세계 사망원인 1위다. 우리나라도 크게 다르지 않다. 심혈관질환은 암에 이어 국내 사망원인 2위를 기록했다.
심혈관질환으로 인해 전신에 혈액을 공급하는 심장의 기능이 악화된 상태를 심부전이라 한다. 심부전 증상을 완화시키고자 이뇨제, 혈관 확장제 등을 처방하지만 이는 심장의 기능을 회복시키지는 못한다. 심부전을 근본적으로 치료하기 위해서는 심장이식 등이 필요하지만 면역 거부 반응, 합병증 위험, 수혜자에 비해 적은 공여자 등으로 인해 어려움이 있다.
심장질환은 심장의 재생능력이 매우 제한돼 있어 치료가 어렵다. 심장의 주요 역할을 하는 심근세포가 잘 증식하지 않기 때문이다. 심근세포는 태아에서는 활발히 증식하지만 출생 이후 증식능력이 감소하면서 성인에서는 증식을 거의 멈추게 된다.
연구팀은 먼저 심근세포의 증식능력을 감소시키는 유전자를 규명했다. 태아, 신생, 어른 세 가지 마우스모델의 심장에서 세포 주기를 조절하는 폴리콤(polycomb) 그룹 단백질이 어떻게 발현되는지 실시간으로 반응을 분석했다.
그 결과 유전자 Cbx7이 출생 직후 급격히 증가해 성인의 심장에서 높게 유지됐으며, 심근세포의 증식에 영향을 미치는 것으로 나타났다.
연구팀은 이 메커니즘을 마우스모델에 적용해 심근세포의 증식능력을 증가시켜 심장의 재생을 유도할 수 있는지 분석했다.
분석 결과 마우스모델에 Cbx7 유전자를 과발현시켰을 때 심근세포의 증식이 줄어들었다. 반면 Cbx7 유전자를 제거한 마우스모델에서는 심근세포의 증식이 증가하는 것으로 나타났다. 심장마비를 유도한 마우스모델에서도 Cbx7 유전자를 제거했을 때 심장 재생이 일어났다.
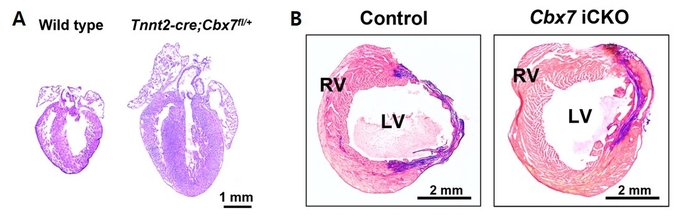
연구팀은 이 과정에서 Cbx7 유전자가 심근세포 증식에 영향을 주는 메커니즘을 발견했다. Cbx7 유전자가 단백질 TARDBP와 결합해 세포 주기를 조절하는 단백질 RBM38의 발현을 유도하는 것으로 나타났다. RBM38의 과발현은 심근세포의 증식을 억제했다.
RNA결합단백질 TARDBP는 mRNA와 결합해 mRNA의 안정성, 이동, 변형 등에 영향을 준다. TARDBP에 의해 영향을 받는 유전자들 중 단백질 RBM38은 Cbx7에 의해 발현이 유도되는 것으로 나타났으며, RBM38은 세포주기를 멈춰 세포의 증식을 억제하는 단백질로 알려져 있다.
윤영섭 교수는 “이번 연구를 통해 Cbx7이라는 유전자가 심근세포의 증식능력과 심장의 재생능력을 조절하는데 중요한 인자임을 밝혔다”면서 “앞으로 Cbx7 저분자 억제제의 심장 재생 효과를 규명한다면 심부전 치료제 개발이 가능할 것으로 기대한다”고 말했다.
관련기사
- 전문질환 제외된 ‘심부전’, 병원도 환자도 볼모 신세 2025-09-15
- “심부전 중증도 B군 유지, 심부전 전공 의사 사라질 수도” 2025-03-25
- 심혈관질환 논의에 ‘심부전’은 없다…갈 길 먼 중증도 상향 2024-11-25
- 심부전, 중중질환 분류∙지속적으로 치료 가능한 체계 필요 2024-11-23
- 라트로필린-2 결손, ‘확장성 심근병증’을 유발한다? 2024-11-20
- 심부전 환자 대상 한약·침 치료 병용 시 치료 효능↑ 2024-09-09
- 엔트레스토, 유럽심장학회서 심부전 증상 개선 및 위험 감소 효과 재확인 2024-05-30
- 당뇨병 환자, 저체중 지속될수록 심부전 발생 위험 61%로 상승 2024-05-28
- 당뇨병 치료제서 심부전 의한 판막합병증 ‘약물치료법’ 찾았다 2024-05-14
- 림프관정맥문합술, 심부전 위험 20~30% 높인다 2024-02-27
- 충남대병원 안수연 전임의, 2023 대한심장학회 젊은연구자상 수상 2023-10-27
- 암보다 사망률 높은 ‘심부전’ 예방·관리법은? 2023-06-30
- 세브란스병원, 소아 심부전 환우회 ‘아이언 차일드’ 행사 개최 2023-05-24
- [인사]고대 안암병원 진윤태 교수, 대한소화기암연구학회 신임 이사장 취임
- [인사]연세대학교 의료원 인사(4/1)
- [동정]이대목동병원 정수연 교수, 대한후두음성언어의학회 ‘예송학술상’ 수상
- [동정]IVI 초대 사무총장 존 클레멘스 박사, 2026 캐나다 가드너상 수상
- [동정]고대 안암병원 정웅교 교수, 대한견·주관절의학회 최우수 학술상 수상
- [동정]고대 구로병원 이유정 교수, ‘제3회 의료진 의료기기 아이디어 쇼케이스’ 장려상 수상
- [동정]서울대병원 이은영 교수, 제30회 JW중외학술대상 수상
- [인사]메디톡스, 개발본부 총괄에 이태상 상무 영입
- [인사]마크로젠, 이응룡 신임 대표이사 선임…‘3인 각자대표 체제’ 출범
- [인사]우정바이오, 신임 대표이사에 문병석 콜마홀딩스 기술연구원장 선임
- [인사]고대 안암병원 진윤태 교수, 대한소화기암연구학회 신임 이사장 취임
- [인사]연세대학교 의료원 인사(4/1)
- [인사]메디톡스, 개발본부 총괄에 이태상 상무 영입
- [인사]마크로젠, 이응룡 신임 대표이사 선임…‘3인 각자대표 체제’ 출범
- [인사]우정바이오, 신임 대표이사에 문병석 콜마홀딩스 기술연구원장 선임
- [인사]연세대학교 의료원 인사(4/1)
- [인사]경희대학교병원 인사
- [인사]경희대한방병원 이재동 교수, 대한한의학회 제40대 회장 취임
- [인사]라이트재단, 이민원 신임 대표이사 취임
- [인사]신장학회 박형천 이사장, 아시아-태평양신장학회 이사장 취임
- [동정]이대목동병원 정수연 교수, 대한후두음성언어의학회 ‘예송학술상’ 수상
- [동정]IVI 초대 사무총장 존 클레멘스 박사, 2026 캐나다 가드너상 수상
- [동정]고대 안암병원 정웅교 교수, 대한견·주관절의학회 최우수 학술상 수상
- [동정]고대 구로병원 이유정 교수, ‘제3회 의료진 의료기기 아이디어 쇼케이스’ 장려상 수상
- [동정]서울대병원 이은영 교수, 제30회 JW중외학술대상 수상
- [동정]메디컬에이아이, 심장학회 ‘디지털 헬스 어워드’ 신설
- [동정]한림대한강성심병원 허준 병원장, 보건복지부장관 표창 수상
- [동정]부산대병원 목정하 교수, ‵결핵예방의 날‵ 대통령 표창 수상
- [동정]순천향대 부천병원 이영구 교수, 대한스포츠의학회 ‘제마스포츠의학상’ 수상
- [동정]길병원 이시훈 교수, AOCE 2026 최우수 연제상 수상