무허가 의료기기 의원납품 업체 2곳 형사고발
표시미기재 수입업체 3곳 1개월 판매업무정지 처분
- 임설화 기자 shlim@medifonews.com
- 등록 2010-08-17 10:55:36
해외학회에 참석해 의료기기를 무단으로 국내에 반입하고 의원 등에 납품한 업체가 형사고발됐다.
식품의약품안전청(청장 노연홍)은 지난 6월 24일부터 8월 4일까지 지자체 의료기기감시원과 합동으로 전국 성형외과, 피부과 등 194개 의료기관의 주름개선에 사용되는 필러형태 조직수복용(생체)재료 사용실태를 점검했다.
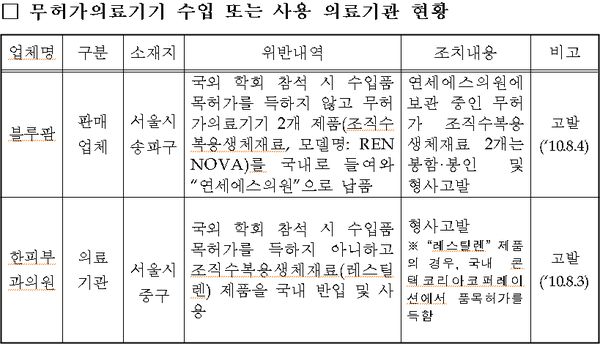
이번 실태조사를 통해 무허가 수입 조직수복용생체재료(모델명: RENNOVA fill(lift)) 2개를 국내에 반입해 의료기관으로 유통한 의료기기 판매업체 블루팜을 적발, 형사고발 조치하고 해당 제품을 봉함했다.
또 조직수복용생체재료(형명 :레스틸렌) 제품 6개를 정식 수입품목허가 절차 없이 핸드캐리로 국내로 들여와 사용한 한피부과의원에 대해 의료기기법 위반으로 형사고발했다. 현재 레스틸렌은 국내 콘택코리아코퍼레이션에서 정식 품목허가를 받은 제품이다.
이와함께 품목허가번호 등 표시사항이 미기재된 Varioderm(수허09-601호) 등 3개 조직수복용생체재료가 11개 의료기관에 사용 중인 것을 확인하고 해당 제품을 수입한 3개 업체에 대해 당해품목판매업무정지 1월의 행정처분을 내릴 방침이다.
표시사항 미기재로 적발된 업체는 △(주)드림파마 조직수복용생체재료(수허09-601호, Varioderm) △(주)디앤컴퍼니 조직수복용재료(수허06-866호, radiesseTM) △(주)그린코스코 조직수복용생체재료(수허10-288호, Stylage M)다.
현행 의료기기법에서는 제조수입 의료기기의 경우, 외관 또는 포장에 반드시 의료기기 품목허가(신고)여부를 확인할 수 있는 ‘품목허가(신고)번호, 형명, 제조번호와 제조원의 상호’를 표시하도록해 사용자가 제품에 대한 정보를 알 수 있도록 의무화하고 있다.
식약청은 의료기관을 포함한 취급자들에게 의료기기 사용 시 품목허가여부를 반드시 확인해 줄 것을 당부했다.
한편 조직수복용생체재료 등 의료기기의 품목허가(신고) 세부 사항은 ‘의료기기제품정보방(www.md.kfda.go.kr)’에 들어가면 확인할 수 있다.
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]순천향대 부천병원 문종호 교수, ‘제19대 대한췌장담도학회 이사장’ 취임
- [인사]SK바이오, R&D 실행력 강화 위해 연구지원조직 정비 및 핵심인재 영입
- [인사]화순전남대병원 김인영 교수, 대한정위기능신경외과학회장 선임
- [인사]원광대병원 김정우 교수, 대한견주관절학회 제34대 회장 취임
- [인사]일동제약그룹 정기승진인사 (4/1)
- [인사]한국산텐제약, 신임 대표이사에 김진희 대표 선임 (4/1)
- [인사]일동제약, 새 R&D 본부장 박재홍 사장 선임
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [동정]가정의학과의사회 유승호 공보이사, 보건복지부 장관상 수상
- [동정]경북대병원 김혜정 연구교수·박준석 교수 연구팀, 대한대장항문학회 ‘우수포스터상’ 수상
- [동정]길병원 노영 교수, 치매 연구 공로, 보건의 날 맞아 복지부 장관 표창













