2분기 임상시험, 1상 승인 최다…2상 최저
1상에서는 국내사가, 3상으로 갈수록 다국적 제약사가 우세
- 노영희 기자 nyh2152@medifonews.com
- 등록 2023-07-01 05:54:45
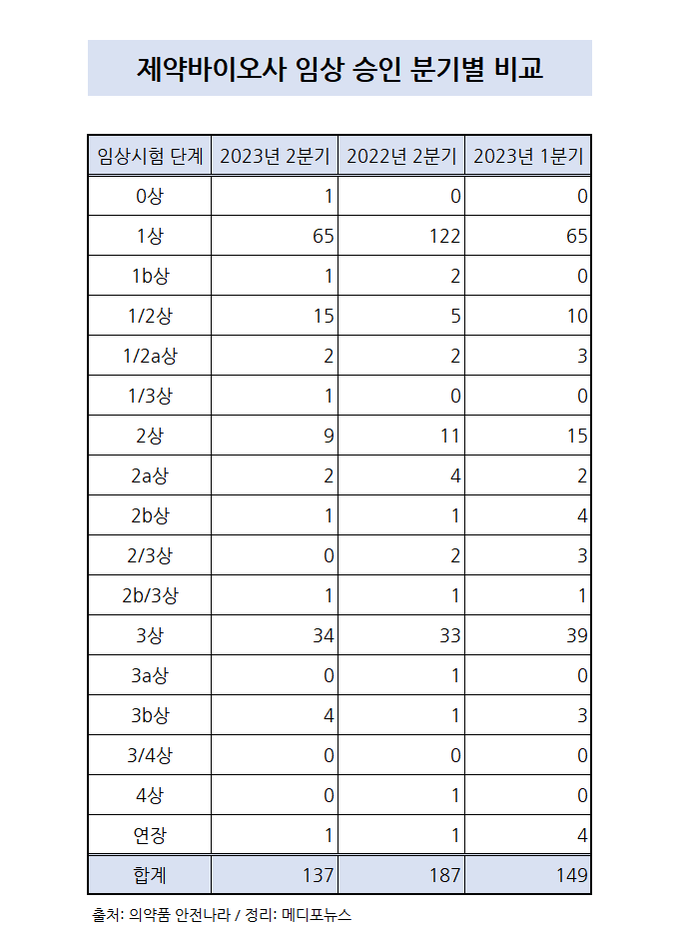
2023년 2분기 주요 제약바이오사들의 임상 승인이 총 143건 이뤄진 것으로 나타났다.
0상이 1 건, 1상 이상 2상 미만이 84건, 2상 이상 3상 미만이 13건, 3상 이상 4상 미만이 39건이었으며 연장 단계의 임상이 1건이었다.
세부적으로는 1상 이상 2상 미만 승인이 많고 3상 이상 승인이 비교적 적은 추세가 이어졌지만 특히 2상 이상 3상 미만 승인 현황은 최저치를 기록했따.
식품의약품안전처가 제공하는 의약품 안전나라 서비스를 통해 2분기 임상시험 승인 현황이 확인됐다.
1상 미만 2상 미만의 단계에서는 국내 제약사가 강세를 보였다. 보령과 종근당이 각각 7건씩 승인을 받은 데에 이어 동구바이오제약도 5건의 임상 승인을 획득했다.
보령의 임상승인 중 제품별로는 BR6002, BR3006, BR1015, BR2015, BR20216가 임상시험에 진입했다.
대표적으로 BR1015-1는 BR1015-2와의 임상시험이 진행됐으며 이는 건강한 성인 자원자를 대상으로 ‘BR1015’ 단독투여와 ‘BR1015-1’ 및 ‘BR1015-2’ 병용투여 시 약동학과 안전성을 비교∙평가하기 위한 공개, 무작위배정, 식후, 단회 경구 투여, 2군, 2기, 교차설계한 임상시험이다. 동일한 약물의 식후, 4기라는 조건의 차이를 둔 임상시험 또한 승인됐다.
BR2016은 건강한 성인에서 ‘BR2016’과 ‘BR2016-1’ 투여 시 약동학 특성과 안전성을 비교 평가하기 위한 공개, 무작위배정, 공복, 단회, 경구 투여, 2군, 2기, 교차설계의 제 1상 임상시험으로 승인됐다.
종근당은 CKD-341, CKD-383, CKD-379, CKD-828, CKD-378 등 5개 약물에 대한 7개 임상시험이 승인받았다.
CKD-341은 건강한 성인 자원자를 대상으로 D958과 CKD-341 투여 시 안전성과 약동학적 특성을 비교 평가하기 위한 1상 임상시험을, CKD-383은 건강한 성인을 대상으로 CKD-383 투여시와 CKD-501, D745, D150 및 D029 병용투여시 약동학적 특성 및 안전성을 평가하기 위한 무작위배정, 공개, 식후, 단회 경구 투여, 2군 2기 교차 임상시험을 승인받았다.
동구바이오제약은 DSM, OEM, OOF 등 3개 약물 5개 임상시험을 승인받았다.
DSM은 ‘DSM’ 단독투여와 ‘DSM-A’와 ‘DSM-B’의 병용투여 시 약동학적 특성과 안전성을 비교평가하기 위한 건강한 성인에서의 공개, 무작위배정, 식후, 단회, 경구 투여, 2군, 2기, 교차, 1상 임상시험으로 같은 조건에서 공복 상태였을 때의 임상시험을 함께 승인받았다.
OEM은 OEM 단독투여와 ‘OEM-A’와 ‘OEM-B’의 병용투여 시 약동학적 특성과 안전성을 비교평가하기 위한 건강한 성인에서의 공개, 무작위배정, 식후, 단회, 경구 투여, 2군, 2기, 교차, 1상 임상시험이었으며 DSM과 마찬가지로 공복을 기준으로 한 임상시험도 함께 승인됐다.
2상 이상 3상 미만에서는 다국적 제약사의 활약이 제법 눈에 띈다. GSK, 사노피-아벤티스, 노바티스, 로슈, 아스트라제네카, MSD 등 다양한 외자사들이 2상 이상에서 임상시험을 승인받았다.
한국로슈의 RO7247669는 이전 치료 경험이 없는 PD-L1 양성, 국소 진행성 절제불가 또는 전이성 삼중 음성 유방암 시험대상자에서 냅-파클리탁셀과 병용한 펨브롤리주맙 대비 냅‑파클리탁셀과 병용한 RO7247669를 평가하는 제2상, 다기관, 무작위배정, 이중눈가림 시험으로 2상 승인을 받았다.
한국아스트라제네카의 MEDI5752, AZD2936는 진행성 간담도암 환자를 대상으로 단일요법 및 항암제와의 병용요법으로서 면역조절제 신약의 유효성과 안전성을 평가하기 위한 제2상, 공개라벨, 다중약제, 다기관, 마스터 계획서로 허가를 받았다.
3상 이상으로는 총 40건의 승인 현황이 확인됐다. 3상 이상부터는 다국적 제약사의 승인 비중이 훨씬 더 높게 나타났다.
한국얀센 4건을 비롯해 한국애브비, 한국릴리, 바이엘코리아 등이 각각 3건씩 임상시험을 승인받았다.
먼저 한국얀센의 ‘밀벡시안정25mg’은 급성 허혈성 뇌졸중 또는 고위험 일과성 허혈 발작 후 뇌졸중 예방을 위한 경구용 11a 혈액응고인자 억제제(Factor XIa Inhibitor)로 밀벡시안의 유효성 및 안전성을 입증하기 위한 제3상, 무작위배정, 이중 눈가림, 평행군, 위약 대조 시험(LIBREXIA-STROKE)으로 승인을 받았다.
한국릴리의 제품 중 ‘LY3502970’은 심혈관계 위험이 높은 비만 또는 과체중에 해당하는 제2형 당뇨병 성인 시험대상자에서 인슐린 글라진과 비교한 LY3502970 1일 1회 투여의 제3상, 공개 시험 (ACHIEVE-4)으로 임상이 진행된다.
한국애브비의 임상 3건은 모두 ABT494와 관련한 임상으로, 류마티스관절염, 활성 SLE 환자, 화농성 한선염 등 다양한 적응증에 대한 임상시험을 승인받았다.
바이엘코리아의 임상시험 중 2건은 ‘BAY 1747846’ 임상시험으로, 그 중 한 건은 신체 부위(CNS 제외)에 알려졌거나 의심되는 병리가 있는 성인을 대상으로 MRI용 0.04 mmol Gd/kg(체중)의 가도콰트란(gadoquatrane)의 유효성과 안전성을 승인된 0.1 mmol Gd/kg의 거대고리 가돌리늄 기반 조영제(GBCA)와 비교해 평가하기 위한 다기관, 무작위배정, 전향적 이중눈가림으로 진행된다.
다른 한 건은 중추신경계(CNS)에 알려졌거나 의심되는 병리가 있는 성인을 대상으로 MRI용 0.04 mmol Gd/kg(체중)의 가도콰트란의 유효성과 안전성을 승인된 0.1 mmol Gd/kg의 거대고리 가돌리늄 기반 조영제(GBCA)와 비교해 평가하기 위한 다기관, 무작위배정, 전향적 이중눈가림, 교차 제3상 임상시험으로 진행된다.
관련기사
- 1분기 주요 제약바이오사 임상 134건 승인…3상 이상이 34% 2024-04-02
- 4분기 ‘3상’ 임상승인 최다…출시 기대 약물은? 2024-01-02
- 3분기 임상승인 129건 중 과반이 1상에…어떤 약물 탄생될까 2023-10-04
- 1분기, 임상 승인건수 적지만 ‘3상 이상’ 우세 2023-04-04
- 4분기, 3상 임상승인 ‘최다’…2023년 출시 임박한 약은? 2023-01-02
- 갈수록 줄어드는 임상 승인, 3분기는 승인건수는 179건 2022-10-04
- 넥스트 국산 백신, 유바이오로직스가 탄생시킬까 2022-09-08
- ‘출시 기대’ 3상 승인된 코로나19 백신·치료제 총 4건 2022-07-11
- 2분기 임상시험 승인 건수는 소폭 감소된 187건 2022-07-04
- 1분기 임상시험 총 288건…작년 대비 1상 증가 2022-04-04
- 임인년 맞아 출시를 기대할 만한 신약은? 2022-01-03
- 3분기 임상시험 총 312건 진행…1·2·3상 모두 증가 2021-10-02
- 2분기 임상 총 286건…1상 늘고 2·3상 감소 2021-07-02
- 제약바이오사 2분기 임상시험, 진행상황은? 2020-07-20
- 서울대병원, 세계적 임상센터의 중심에 서다! 2010-10-12
- 국가임상시험사업단-애보트 MOU 협약 2010-10-08
- 정신질환자 임상시험 중 돌연 자살 '의혹 제기' 2010-10-04
- FDA, 임상시험 중 부작용 즉각 보고규정 마련 2010-10-02
- 서울대병원, 차세대 스텐트 임상시험 대규모 진행 2010-07-19
- 국내 임상시험 “약진”, 다국가 임상시험보다 앞서 2009-11-13
- 국내사 ‘1상’-다국적사 ‘3상임상’ 가장 많아 2009-08-04
- 신풍제약 ‘록스펜주’ 등 임상시험 6건 승인 2008-12-13
- “임상시험 등 각종 시험관련 의견 보내주세요” 2008-07-30
- 응급시 임상시험용약 사용 완화-승인기간 단축 2008-06-19
- [인사]보건복지부 인사(4/26)
- [인사]제약협회, 홍보전문위원장에 최천옥 한림제약 상무 재추대
- [인사]건일제약, 오인수 신임 마케팅본부장 영입
- [인사]삼천당제약 2024년 정기승진인사 (4/23)
- [인사]오태윤 강북삼성병원 교수, 의료기관평가인증원 제6대 원장 임명
- [인사]한미사이언스, 노용갑 부회장 영입
- [인사]사노피 배경은 대표, 한국 및 호주/뉴질랜드 제약 총괄 다국가 리드 선임
- [인사]연세대학교의료원 인사
- [인사]서울성모병원 오득영 교수, 대한미용성형외과학회 이사장 취임
- [인사]고대 안암병원 함병주 교수, 대한생물정신의학회 이사장 취임
- [동정]전북대병원 이선영 교수팀, 국제학술지 ‘Cancers’ 에 논문 게재
- [동정]암젠, 아동·청소년 생명과학 교육 캠페인 서울시장 표창 수상
- [동정]칠곡경북대병원 성인 수두증 클리닉, 30억원 치매극복 기술개발 과제 수주
- [동정]갑상선 수술 관련 비디오 후두경 통한 기관삽관 유용성 입증
- [동정]한국머크 바이오파마, ‘일∙가정 양립 우수 기업’ 선정
- [동정]고대 구로병원 송준영 교수, 질병청·국립보건연구원 학술연구용역 과제 선정
- [동정]일동후디스 하이뮨, 브랜드파워 단백질보충제 부문 2년 연속 1위
- [동정]서울성모병원 정미향 교수, 국제학술지 유럽예방심장학회지 부편집장 임명
- [동정]한올바이오파마, 국가산업대상 ‘연구개발’ 부문 수상
- [동정]제주대병원 연구팀, 국제학술지에 심장재활 논문 게재















