't'검색결과 - 전체기사 중 2,669건의 기사가 검색되었습니다.
상세검색-

상하이 콩코디아 국제학교, 세계 최고의 학교상 톱 10 후보에 선정됨
-- 콩코디아 상하이, 건강한 삶 지원 부문 세계 최우수 학교상 최종 후보 10곳에 선정돼었다. 상하이 2024년 6월 17일 /PRNewswire=연합뉴스/ -- 중국의 한 국제학교가 2024년 세계 최우수 학교상(World's Best School Prizes) 상위 10개 후보에 이름을 올렸다. T4 에듀케이션이 액센츄어, 아메리칸 익스프레스, 레만 재단과 공동으로 설립한 세계 최고 학교상 5개 부문은 세계에서 가장 권위 있는 교육상이며 올해 수상자에게는 5만 달러의 상금이 수여된다. Concordia International School Shanghai Named in Top 10 Shortlist for World’s Best School Prizes 건강하고 연합된 커뮤니티를 조성하고 교직원 복지를 증진하며 학생들의 성공을 향상시키는 중국 상하이의 독립적인 유치원부터 고등학교까지 운영하는 콩코디아 국제학교 상하이가 건강한 삶을 지원하는 세계
- PR Newswire
- 2024.06.17 15:38
-

HK이노엔, 3사 공동개발 자가면역질환 이중항체 신약 美기술이전
HK이노엔(대표 곽달원)은 아이엠바이오로직스(대표 하경식)와 와이바이오로직스(각자대표 박영우·장우익) 3사가 공동으로 개발한 OX40L항체와 TNF-α(종양괴사인자-α) 타깃 이중항체 신약 후보물질 ‘IMB-101(OXTIMA)’이 미국 신약 개발 전문 기업에 기술이전 됐다고 17일 전했다. 계약 규모는 계약금 2,000만 달러(한화 약 276억 원)를 포함해 총 9억 4,000만 달러(한화 약 1조 3천억 원)이며, 이번 기술이전 계약은 아이엠바이오로직스 주도 아래 성사됐다. 계약 지역은 아시아를 제외한 글로벌(일본 포함) 지역이다. HK이노엔은 계약조건에 따라 총 계약 규모의 일정 비율 수익금을 수령하며, 총 계약 규모 외 출시 후 매출에 따른 로열티도 별도 수령한다. 이번 기술을 이전받은 미국 ‘내비게이터 메디신(Navigator Medicines)’은 OX40-OX40L 시그널 저해제를 집중 개발하는 기업으로, 미국의 대형 벤처캐피탈인 RA 캐피털매니지먼트(RA Capital Management)의 투자를 받은 바 있다. IMB-101은 OX40L항체와 TNF-α(종양괴사인자-α)를 동시에 타깃해 주요 염증성 사이토카인과 T-세포를 동시에 제어하는 자
- 노영희 기자
- 2024.06.17 14:24
-
오노-BMS ‘옵디보’, ASCO 2024에서 다양한 암종 최신연구결과 발표
한국오노약품공업과 한국BMS제약은 5월 31일부터 6월 4일까지 열린 미국임상종양학회 연례학술대회(ASCO 2024)에서 간세포암, 비소세포폐암, 대장암 등 다양한 암종에 걸쳐 옵디보(성분명:니볼루맙) 기반 요법의 유효성 및 안전성을 확인한 새로운 임상 연구 결과를 발표했다. ◆옵디보-여보이 병용, CheckMate-9DW 연구서 절제 불가능한 간세포암 1차 치료 유효성 확인 이전에 전신 치료를 받지 않은 절제 불가능한 간세포암 환자 668명을 대상으로 옵디보-여보이(성분명: 이필리무맙) 병용요법과 렌바티닙 또는 소라페닙 투여군을 비교 평가한 임상 3상 CheckMate-9DW 연구의 첫 번째 결과가 3일(현지시간) ASCO 2024에서 공개됐다. 연구의 1차 평가 변수는 전체 생존율(Overall Survival, OS)이며, 주요 2차 평가 변수로는 객관적 반응률(Objective Response Rate, ORR)과 증상 악화까지의 시간 그리고 반응 지속 기간(Duration of Response, DoR) 등이 포함됐다. 추적 관찰 기간 중앙값 35.2개월의 연구 결과, 옵디보-여보이 병용요법을 3주 간격으로 최대 4사이클 실시한 후, 옵디보 단독요법
- 노영희 기자
- 2024.06.17 09:15
-

테라펙스, 4세대 EGFR 비소세포폐암 치료제 임상1상 첫 환자 투약 개시
테라펙스(대표이사 이구)는 EGFR 비소세포폐암 표적항암제 'TRX-221'의 국내 임상 1상 첫 환자 투약을 삼성서울병원에서 시작했다고 17일 밝혔다. 테라펙스는 미국 FDA에서 승인된 임상시험계획(IND)에 따라, EGFR 변이 비소세포폐암 환자 가운데 기존 세대 EGFR 저해제 중 하나 이상의 치료제를 투약 받은 후 질병이 진행된 환자 115명을 대상으로 TRX-221의 안전성과 효능을 탐색한다. TRX-221의 임상 1/2상 시험은 3단계로 진행될 예정이다. 1a상 용량 증량 단계에서는 단계적 약물 증량을 통한 약물의 안전성(safety) 및 내약성(tolerability)을 평가하게 되며, 1b상 용량 탐구 단계에서는 약물의 최대내약용량 또는 2상 시험용 추천용량(RP2D)을 결정하게 된다. 마지막으로 2상에서는 고형암 평가 기준(RECIST) 버전 1.1을 토대로 약물의 객관적 반응률(Objective Response Rate, ORR)을 통해 TRX-221의 약효를 평가하고 약물에 의한 부작용 등을 탐색하게 된다. 테라펙스는 임상 시험 가속화를 위해 1상 용량 증량 단계는 삼성서울병원 등 국내 6개 병원에서 진행하고, 용량 탐구 단계부터는 환자
- 노영희 기자
- 2024.06.17 09:03
-

지노믹트리, 방광암 진단 제품 ‘얼리텍-B’ 확증임상 성능시험에서 유효성 입증
지노믹트리(대표이사 안성환)는 방광암 조기진단을 위한 ‘얼리텍-B’ 체외 분자진단 제품의 한국 식품의약품안전처 제조 허가 획득을 위한 확증 임상적 성능시험(NEXT-BC)에서 유효성을 입증했다고 14일 밝혔다. 이번 임상시험은 혈뇨 환자들을 대상으로 방광암 진단에 대한 ‘얼리텍-B’ 진단법 효력을 평가하기 위해 설계됐다. 임상시험은 ‘얼리텍-B’ 검사를 통해 예후가 나쁜 방광암 환자 식별 성능에 대한 통계적 유효성을 평가하는 것을 주요 목적으로 진행됐다. 부가적인 목적으로는 기존에 상용적으로 사용하고 있는 다른 진단법들과의 비교분석과 전체 방광암에 대한 진단적 민감도 및 특이도를 유효성 평가변수로 설정했다. 이번 확증임상시험 데이터를 분석한 결과, 예상한 성능이 통계적으로 유효성이 입증됐다. 얼리텍-B는 방광암 조기진단용 바이오마커로, 자체 발굴하고 검증한 ‘PENK 메틸화’ 유전자를 대상으로 검출 민감도를 최적화시킨 독창적인 측정 기술인 ‘LTE-qMSP’ 방법을 사용해 방광암을 진단한다. 이 기술은 소변 속 바이오마커를 민감하게 측정해 방광암을 정확하게 진단할 수 있는 새로운 체외 분자진단 기술로, 미국 FDA와 한국 식품의약품안전처로부터 혁신의료기기로
- 노영희 기자
- 2024.06.14 10:54
-

옥타파마, 희귀 출혈 장애 환자들의 삶을 개선하기 위한 동사의 지속적인 헌신을 ISTH 202에서 쇼케이스
옥타파마는 곧 있을 ISTH 2024 콩그레스에서 윌레이트®와 뉴위크®에 대한 새로운 임상 및 과학 연구 결과를 발표 새로운 데이터와 임상 연구 개발 결과를 7개의 구두 프리젠테이션, 2개의 포스터와 2개의 지원 심포지엄에서 쇼케이스 라헨, 스위스, 2024년 6월 11일 /PRNewswire/ -- 옥타파마(Octapharma)의 혈액 포트폴리오 중에서 가장 최근에 개발된 제품들이 2024년 6월 22일부터 26일까지 태국 방콕에서 열리는 제32차 국제 혈전증 및 지혈 학회(ISTH) 콩그레스에서 발표된다. 본 데이터는 이 주요 국제 회의에서 열릴 7개의 구두 프리젠테이션, 2개의 포스터와 2개의 지원 심포지엄에서 공개된다. 옥타파마는 ISTH 2024년 콩그레스의 자랑스러운 실버 서포터이다. 또한 옥타파마는 중환자와 응급 환자들의 급성 출혈과 응고 처치를 위해 제공하는 현대적인 솔루션들을 발표한다. A형 혈우병과 폰빌레브란트병(VWD)과 같은 출혈 장애는 반복적이고 장기적인 출혈의 위험을 안고 있으며, 생명을 위협할 뿐만 아니라 환자의 삶의 질과 정신 건강에도 큰 장
- PR Newswire
- 2024.06.11 19:45
-

멀츠 에스테틱스 코리아, 스킨 퀄리티 주제 MEX 웨비나 성료
멀츠 에스테틱스 코리아(대표 유수연, 이하 멀츠)가 지난 6월 7일 멀츠 에스테틱스가 운영하는 정기 학술 교육 프로그램인 ‘MEX 웨비나(Merz Experts Webinar)’를 성료했다고 밝혔다. 22회차를 맞은 이번 MEX 웨비나에서는 모델로피부과 서구일 원장의 진행 아래 독일 로젠파크(Rosenpark) 클리닉의 소냐 새틀러(Sonja Sattler) 박사와 압구정오라클피부과 박제영 대표원장의 스킨 퀄리티에 대한 강의와 토론이 진행됐다. 강의 후 진행된 토론 세션에서는 스킨 퀼리티와 관련한 글로벌 에스테틱 트렌드와 병용치료를 주제로 활발한 논의가 이어졌다. 첫 번째 연자를 맡은 새틀러 박사는 최근 국제학술지 ’피부미용임상연구(Clinical, Cosmetic and Investigational Dermatology, CCID)’에 게재된 논문 ‘스킨 퀄리티 – 전체적인 360° 관점: 합의된 결과(Skin Quality – A Holistic 360° View: Consensus Result)’와 관련해 설명하며 “스킨 퀄리티는 매력을 높이는 주요한 요소인데, 그동안은 우수한 스킨 퀄리티에 대한 표준화된 기준이 없었지만, 이번 논문을 통해 전세계적인
- 노영희 기자
- 2024.06.11 10:53
-

LG화학, 차세대 면역관문억제제 개발로 고형암 치료 솔루션 제공 나서
LG화학이 고형암 환자들의 치료 기회 확대를 위한 차세대 면역관문억제제 임상 개발에 본격 착수한다. LG화학은 11일, 첫 자체 개발 항암신약 물질인 ‘LB-LR1109(연구과제 코드명 LR19155)’ 미국 임상 1상에 시험자를 등록했다고 밝혔다. 이 후보물질은 ‘LILRB1(Leukocyte Immunoglobulin Like Receptor B-1)’ 억제 기전의 단일 항체 약물로 다양한 면역세포에서 발현되는 면역관문(면역계 회피) 신호 분자인 ‘LILRB1’과 암세포에서 발현돼 면역세포의 공격을 막는 단백질인 HLA-G(Human Leukocyte antigen-G)의 결합을 방해해 체내 면역세포 전반의 기능을 동시다발적으로 활성화하는 역할을 한다. LG화학은 타깃 단백질인 ‘LILRB1’이 대표적 면역세포인 T세포뿐만 아니라 NK세포(자연살해세포), 대식세포(식균세포) 등 다수 면역세포의 표면에 공통으로 발현된다는 점에서 T세포 등 단일 면역세포 작용에만 초점을 맞춘 기존 면역관문억제제와 뚜렷한 차별점이 있다고 설명했다. LG화학은 고형암 동물모델에서 용량 의존적 항암 효과 등을 확인했으며, 이를 바탕으로 지난해 12월 미국 식품의약국(FDA)으로부
- 노영희 기자
- 2024.06.11 09:39
-

위암별로 고령환자 생존에 유리한 첫 치료법은?
국내 75세 이상 위암 고령환자의 치료법 이용 현황 및 예후 근거가 제시됐다. 한국보건의료연구원(NECA)이 국내 노인 위암환자에서 첫 치료법 이용 현황과 치료법에 따른 생존 예후를 분석한 연구결과를 6월 10일 발표했다. 한국보건의료연구원 박동아 선임연구위원과 국립암센터 국립암데이터센터‧암빅데이터센터 최귀선 센터장은 국가암데이터를 이용해 ‘노인 위암환자에서의 수술치료 효과 및 국내 근거창출 연구’를 수행했다. ◆75세 이상 위암 환자의 첫 치료법 이용 현황 연구팀은 2014~2019년 맞춤형 암 공공 라이브러리를 이용해 75세 이상 위암 환자 3만6099명의 치료 현황을 분석했다. 암 진단 후 환자가 받은 첫 번째 치료는 위절제술(34.5%)이 가장 많았고, 이어 내시경적 점막하박리술(ESD) 23.1% > 항암화학요법 4.3% > 방사선치료0.5% 순으로 집계됐다. 위암 병기에 따라 치료 현황을 살펴보면, ▲암이 위에만 있는 환자(국한 위암)는 ESD(41.8%)를 ▲위 주위 장기나 조직에 직접 침범한 환자(국소 진행 위암)는 위절제술(63.1%)을 ▲원격 전이가 진행된 환자(원발 전이 위암)는 항암화학치료(22.1%)를 각각 첫 치료로 이용했
- 김민준 기자
- 2024.06.10 13:59
-

파킨슨병 환자들을 위한 가능성 있는 애드온 치료: 스팀비아, 시범 연구를 끝내고 긍정적인 초기 결과를 발표
프라하, 2024년 6월 7일 /PRNewswire/ -- 만성질환 치료를 위한 신경조절을 전문으로 하는 선구적인 의료 기술 기업 스팀비아(Stimvia)가 파킨슨병(PD)에 초점을 맞춘 시범 연구를 성공적으로 끝내고 긍정적인 결과를 기대하고 있다. The URIS® device operates on a principle of electrical transcutaneous nerve modulation (eTNM®). 본 연구의 책임자이자 오스트라바 대학 의대 과학 및 연구 담당 부학장 데이비드 스콜루딕(David Scoloudik),MD, Ph.D.,FESO, FEAN 교수는 "우리는 긍정적인 결과를 의미하는 예비 결과를 발표하게 되어 기쁘게 생각한다"면서 "환자들은 파킨슨병 증상의 가지 수와 전반적인 삶의 질 모두에서 개선되었다고 보고했다. 게다가, 우리는 안정 시 떨리는 증세가 크게 감소하는 것을 관찰했다. 정확한 데이터는 여전히 엄격한 평가가 필요하지만, 우리는 이러한 결과가 함축하는 가능성에 대해 조심스럽게 낙관하고 있다"고
- PR Newswire
- 2024.06.08 09:00
-

항암요법연구회, ASCO 2024에서 한국 의료진 연구 역량 입증
대한항암요법연구회(회장 장대영)는 지난 5월 31일부터 오는 6월 4일까지(현지 시각) 미국 시카고에서 온오프라인으로 개최된 미국임상암학회 연례학술대회(American Society of Clinical Oncology 2024, 이하 ASCO 2024)에서 대한항암요법연구회 회원이 제1 저자로 참여한 연구가 58건 발표됐으며, 이 중 7건이 구연 발표였다고 밝혔다. 아울러 국내 연구자들이 참여한 구연 및 포스터 발표는 174건에 달했으며, 대한항암요법연구회 연구과제로 수행된 연구는 7건이었다. 장대영 회장은 “연구개발 비용의 증가와 규제 환경의 변화로 한국을 비롯한 아시아 국가의 임상연구 수가 감소세를 보이는 와중에도, 올해 ASCO에서 대한항암요법연구회 연구과제로 채택된 연구와 한국인이 주 연구자로 참여한 연구는 작년보다 늘어났다는 점을 통해 한국의 임상연구 역량을 재확인할 수 있었다”며, “특히 대한항암요법연구회가 연구과제로 채택한 연구가 구연 발표 및 포스터 세션에 다수 공개되며, 그간 연구가 거의 이루어지지 않았던 희귀암 치료 시장과 바이오마커를 통한 최적의 치료법을 찾는 논의의 장에 유의미한 화두를 던졌다”고 강조했다. 진행성 요막관암 1차 치료에
- 노영희 기자
- 2024.06.04 11:28
-

양산부산대병원, 경남 최초 MRI 6호기 가동식 개최
양산부산대병원은 경남지역 최초 총 6대의 MRI 장비가 설치된 병원이 됐다. 양산부산대병원은 지난 3일 MRI 6호기 장비 도입을 기념해 가동식을 개최했다고 6월 4일 밝혔다. 이날 행사에는 이상돈 병원장을 비롯한 주요 보직자와 GE(General Electric) Health Care 관계자가 함께 참석해 자리를 빛냈다. 양산부산대병원은 경남지역 최초 MRI 장비 6대 설치된 병원이라는 타이틀과 함께 이번에 도입한 MRI 6호기(SIGNA Premier 3.0T)는 양산부산대병원이 경남지역 최초로 국내 최고사양(Ver 30.1)이 탑재된 GE의 프리미엄 최신형 장비를 도입했다는 점에서도 아주 큰 의미를 갖고 있다. 이번에 도입된 ’SIGNA Premier 3.0T‘ 최신형 MRI는 AIR™ Recon DL(AI 학습 알고리즘) 기반 소프트웨어로 반복 스캔을 줄이면서도 일관성 있는 검사와 더 선명한 영상 신호를 획득해 고해상도, 고속 검사가 가능하다. 또 80mT/m으로 하드웨어 성능 향상과 환자의 편의성을 고려해 여러 각도로 움직이지 않아도 가볍고 포근한 이불 형태의 에어 코일(AIR™ Coils)을 이용해 360도 촬영이 가능해져 편안하고 안정적인 검사
- 김민준 기자
- 2024.06.04 09:57
-

새 진료지침 발표 앞둔 후두암, 진료 참고사항은?
연내 새 후두암 진료지침 발표를 앞두고 현재 진료지침 진행상황에 대해 논의하는 시간이 마련됐다. 2024년 대한두경부외과학회 춘계학술대회가 개최된 가운데, ‘후두암 진료지침’ 세션이 열렸다. 해당 세션에서는 첫 순서로 서울성모병원 이비인후과 김상연 교수가 ‘조기후두암’ 연구 결과에 대해 밝혔다. 조기후두암 부문에서는 △조기 성문암(T1/T2)에서 최적의 치료는 무엇인가 △조기 성문상부암(T1/T2)에서 최적의 치료는 무엇인가? 김 교수는 첫 번째 질문에 대해 “전체 생존율에 있어서는 수술군이 비수술군 대비 이득이 있었다. 그러나 비수술군은 보다 위험하기는 했지만, 두 그룹 간의 유익성과 위해성의 실질적인 차이를 파악하는 것은 어려웠다.”며 “두 치료 모두 조기후두암 초기치료로 적용이 가능하다”고 설명했다. 두 번째 질문에 대해서는 “연구에 목 절개를 받은 참가자가 포함돼있었고, 타 연구 대비 추적기간이 1.5년으로 비교적 짧았지만 연구 결과 수술은 방사선 치료에 비해 전반적인 생존율이 더 좋은 것으로 나타났다. 일단은 두 개 치료 모두 초기 치료로 가능하다”고 전했다. 다만 해당 연구들은 수술적 치료와 독점적 방사선 치료 사이의 비교에서 명확한 우월성에 대한
- 노영희 기자
- 2024.06.04 06:00
-
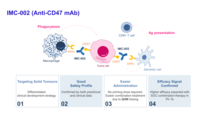
이뮨온시아, ASCO에서 CD47 항체 1상 임상시험 바이오마커 결과 발표
이뮨온시아(대표 김흥태)는 2024년 6월 1일(현지시간) 미국 시카고에서 개최된 미국임상종양학회(American Society of Clinical Oncology, ASCO)에서 CD47 단클론항체 IMC-002의 고형암 임상 1a상 결과 업데이트 및 의료 인공지능(AI) 기업 루닛(대표 서범석)과의 협업을 통해 확인된 바이오마커 결과를 발표했다고 밝혔다. 본 연구는 임상1상 용량 증량(dose escalation) 파트로, 2022년 5월부터 총 4개의 용량 코호트에 12명의 환자가 등록돼 각각 IMC-002 5, 10, 20, 또는 30 mg/kg을 2주 간격으로 투여받았다. 치료 결과 측정 가능한 병변이 있는 환자 12명중 6명에서 안정반응(SD)이 확인돼 50%의 질병조절율(DCR)을 보였다. 이중 5명은 간세포암 환자, 1명은 유방암 환자였다. 또한, 환자 4명에서 6개월 이상 안정반응이 지속돼 33.3%의 임상적 이득율(CBR)이 확인됐다. AI를 활용한 바이오마커 분석(Lunit SCOPE IO) 결과, 임상 효능이 확인된 CBR 그룹의 CD47 양성 대식세포 밀도가 비CBR 그룹에 비해 더 높은 것으로 나타났다 (71.0/mm2 대 44.3
- 노영희 기자
- 2024.06.03 10:16
-

임상재단, 中 상하이에서‘한-중 임상시험 심포지엄’ 성료
18개 국내 제약사가 참여한 ‘한-중 임상시험 심포지엄’(이하 행사)이 성공적으로 개최됐다. 이번 행사는 중국 타이거메드(Tigermed) 및 한국 드림씨아이에스와 협력하에 진행됐다. 국가임상시험지원재단(이사장 박인석, 이하 재단)은 지난 5월 16일부터 18일까지 중국 상하이에서 국내 제약사의 중국 진출을 지원하기 위해 이번 심포지엄을 개최했다고 밝혔다. 행사는 재단이 처음으로 중국 현지에서 개최한 것으로, 중국 규제 및 임상 전략을 공유하고, 현지 임상시험 전문가들과의 네트워킹을 위해 마련됐다. 행사는 중국 상하이 일대에서 2박 3일의 일정으로 진행됐으며, 광동제약, 한미약품, 대웅제약, 보령제약, HK이노엔, JW중외제약, 동국제약, 제뉴원사이언스, 안국약품, 메디톡스, 신풍제약, 종근당 바이오, 유영제약, 삼성제약, 애드파마, 이니바이오, 퓨처캠 등 국내 유수의 제약사 총 18개 기업 35여명의 임상시험 전문가가 참여했다. 참석자들은 첫날, 미국에 본사를 두고 있는 프론티지의 중국 상하이 소재 센트럴 랩 연구소를 방문했다. 중국 NMPA와 미국 FDA 표준에 맞는 실험실 시설, 임상 샘플 분석 시설 등 다양한 연구가 진행되고 있는 랩시설을 둘러보았다.
- 노영희 기자
- 2024.06.01 09:52
-

식약처, 화이자 재발 또는 불응성 다발골수종 치료제 ‘엘렉스피오주’ 허가
식품의약품안전처(처장 오유경)는 한국화이자제약㈜이 수입하는 희귀신약 ‘엘렉스피오주(엘라나타맙)’를 5월 30일 허가했다고 밝혔다. 이 약은 프로테아좀억제제, 면역조절제제, 항-CD38 단클론항체를 포함해 3차 이상의 치료를 받은 재발 또는 불응성 다발골수종 성인 환자에서 단독요법으로 사용한다. 엘렉스피오주는 다발골수종 암세포에서 발견되는 B-세포 성숙 항원(BCMA)과 면역 T 세포에서 발견되는 CD3를 표적으로, 두 가지 세포에 이중 특이적으로 결합해 면역반응으로 다발골수종 암세포를 파괴한다. 식약처는 “이 약이 3차 이상의 치료를 받은 재발 또는 불응성 다발골수종 환자에게 새로운 치료 기회를 제공할 것으로 기대한다”면서“앞으로도 규제과학 전문성을 기반으로 안전성·효과성이 충분히 확인된 치료제가 신속하게 공급될 수 있도록 최선을 다할 예정”이라고 밝혔다.
- 노영희 기자
- 2024.05.30 14:59
-

큐로셀, 차세대 CAR-T 치료제 ‘안발셀’ 최종 임상시험보고서 수령
큐로셀(대표이사 김건수)이 국내 최초로 재발성, 불응성 거대B세포림프종(LBCL) 환자를 위한 차세대 CAR-T 치료제 ‘안발셀(Anbal-cel, CRC01)’의 임상 2상시험 최종결과보고서(이하 ‘CSR’)를 수령했다고 29일 공시했다. 이번에 수령한 CSR에는 지난 3월 공시된 톱라인(Topline) 유효성 결과에 추가로 안전성 결과가 수록됐다. CSR의 주요 내용인 안발셀 임상2상 최종 유효성은 지난 3월 공시한 톱라인 결과와 동일했다. 임상 2상시험 유효성 분석 대상자 73명 중 안발셀 투여 후 암세포가 모두 사라진 완전관해에 도달한 비율(CRR)은 67.1%였다. 임상시험의 성공여부를 판단하는 일차 평가변수인 객관적반응률(ORR)은 75.3%이었으며, 최종 결과는 임상시험 설계 당시 가정했던 통계적 유의성을 확보했다. 또한 이번 CSR을 통해서 안발셀의 최종 안전성 데이터가 최초로 확인됐다. CSR에 수록된 안발셀의 임상 2상에서 관찰된 3등급 이상의 사이토카인방출증후군(이하 ‘CRS’)은 8.9%, 3등급 이상의 신경독성(이하 ‘NE’)는 3.8%였다. 그에 비해 국내에서 유일하게 판매되는 킴리아의 3등급 이상 CRS와 NE 발생률은 각각 23%
- 노영희 기자
- 2024.05.30 14:36
-

바이엘, 아일리아 8mg 국내 허가 기념 ‘파워 심포지엄’ 성료
바이엘 코리아(대표이사 이진아)는 지난 24일, 25일 양일간 그랜드인터컨티넨탈 서울 파르나스에서 자사의 항-혈관내피성장인자(이하 anti-VEGF) 치료제인 아일리아주8밀리그램(Eylea 8mg, 이하 아일리아 8mg)의 국내 허가를 기념하는 '2024 파워(POWER) 심포지엄‘을 성료했다고 30일 밝혔다. 이번 심포지엄에서는 ‘망막 질환 치료 패러다임의 전환점’이라는 주제 아래, 심포지엄 첫 날은 서울아산병원 안과 김중곤 교수, 서울대학교병원 안과 박규형 교수가 좌장을 맡고 둘째날은 한림대강남성심병원 안과 김하경 교수와 누네안과병원 이원기 원장이 좌장을 맡아 그간 anti-VEGF 치료제 분야를 선도하며 지속적인 혁신을 이룩한 아일리아의 역사와 임상적 가치를 재조명했다. 특히 최근 최대 20주까지 투여 간격 연장으로 망막 질환 치료의 새로운 전환점을 마련한 아일리아 8mg의 효능과 안전성 데이터를 중심으로 전문의들의 심도 깊은 의견 교환이 이루어졌다. 심포지엄 첫 날, 장우혁안과의원 장우혁 원장은 '우리는 망막 질환 환자 치료 결과를 최대로 이끌어내고 있는가?‘라는 주제로 발표를 진행했다. 그는 그동안 nAMD(Neovascular age-related
- 노영희 기자
- 2024.05.30 10:24
-

Bened Life, Neuralli™ MP를 통해 글로벌 시장 진출하다
-- 미국 시장 공략 후 전세계로 신경 건강 혁신 솔루션을 제공 프리몬트, 캘리포니아 2024년 5월 29일 / PRNewswire=연합뉴스/ -- 사이코바이오틱(psychobiotic) 분야를 선도하고 있는 Bened life[https://bit.ly/3R27J0J ]가 신경계 질환을 치료하는 최초의 장-뇌 의료용 프로바이오틱인 Neuralli™ MP로 미국 시장을 공략한 후 이제 세계 시장으로 그 저변을 넓히고 있다. 이와 더불어 아시아 시장과 호주 및 뉴질랜드 시장에도 진출해 사랑과 행복을 선사하고 있다. Bened Life enters global market, expanding footprints with Neuralli MP. "장"을 통해 알 수 있는 것 복부의 울렁거리는 느낌은 장과 뇌가 장기와 중추신경계의 양방향 소통인 장-뇌 축[https://bit.ly/4aIkCUO ]을 통해 소통하는 대표적인 증상으로, 이를 통해 장내
- PR Newswire
- 2024.05.29 12:34
-

MGI Tech, 새로운 Customer Experience Center 및 제조 시설 개설
-- 미국 내 입지 확대 기대 보스턴 및 캘리포니아주 산호세 2024년 5월 28일 /PRNewswire=연합뉴스/ -- 생명과학 분야를 선도하는 핵심 도구 및 기술 구축에 전념하는 MGI Tech Co., Ltd.(이하 MGI)가 자회사인 Complete Genomics를 통해 미국 시장에서 사업을 확장한다고 밝혔다. 이를 통해 게놈 기술을 발전시키고 고객에 대한 지원을 한층 더 강화할 수 있게 되었다. 보스턴 인근에 Customer Experience Center를 개설하고 산호세 본사에 320만 달러를 투자하여 새로운 제조 시설을 설립한 것은 MGI의 미국 내 운영을 위한 중요한 이정표가 되었다. 보스턴의 새로운 Customer Experience Center(CEC) 보스턴 인근 프레이밍햄에 위치한 새로운 Customer Experience Center는 MGI가 미국 동부 해안 지역에 첫발을 내디딘 것으로, 이 지역 고객에게 더 빠른 서비스와 지원을 제공할 것으로 기대된다. MGI의 미국 자회사인 Complete Genomics가 운영하는 CEC는 보스턴과 북동부 지
- PR Newswire
- 2024.05.28 10:57
- [인사]질병관리청 과장급 승진 (9/8)
- [동정]크레스콤 ‘2025 Power Korea 대전’서 보건복지부 장관상 수상
- [동정]보령, ‘기술·경영 혁신대전’ 대통령 표창 수상
- [부음]신지훈 서울아산병원 영상의학과 교수 모친상
- [부음]박현승 前 대한의사협회 총무이사 별세
- [인사]국경없는의사회, 자비드 압델모네임 신임 국제회장 취임 (9/5)
- [동정]삼성바이오에피스, 직업능력개발 관련 고용노동부 장관 표창
- [부음]정신 전남대병원장 장모상
- [인사]보건복지부 과장급 전보 (9/3)
- [동정]대구가톨릭대병원 박기영 교수, 아시아-오세아니아 재활의학회 학술대회서 특별강연·연구발표
- [동정]크레스콤 ‘2025 Power Korea 대전’서 보건복지부 장관상 수상
- [동정]보령, ‘기술·경영 혁신대전’ 대통령 표창 수상
- [동정]삼성바이오에피스, 직업능력개발 관련 고용노동부 장관 표창
- [동정]대구가톨릭대병원 박기영 교수, 아시아-오세아니아 재활의학회 학술대회서 특별강연·연구발표
- [동정]콜마비앤에이치, ‘한국ESG경영대상’ 중견기업 대상 수상
- [동정]원텍, 탈모치료기 ‘헤어빔’으로 2025 올해의 브랜드 대상 7년연속 수상
- [동정]세노비스, 멀티비타민·키즈 비타민 ‘2025 올해의 브랜드 대상’ 수상
- [동정]충남대학교병원 강민웅 교수, 장영실상 수상
- [동정]원텍, ‘올리지오 키스’로 2025 올해의 브랜드 대상 2년연속 수상
- [동정]휴젤, ‘웰라쥬’ 2025 올해의 브랜드 대상 수상













