-
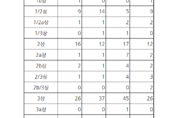
주요 제약바이오사, 초기임상 진입 확대…1상>3상
지난 2025년 4분기, 주요 제약바이오사가 식품의약품안전처로부터 승인받은 임상시험이 115건으로 한 해 동안 500건에 가까운 임상시험이 승인된 것으로 나타났다. 특히 4분기에는 기존 임상시험보다는 1상이상 2상미만의 새롭게 시작된 연구들이 많아 향후 신약개발로 이어질 수 있을지 기대가 모이고 있다. 1상이상 2상미만의 단계에서는 휴온스가 5건으로 가장 많은 임상시험을 승인받았다. HUC2-676 임상시험이 1건, HUC2-588 임상시험이 2건, HUC3-660 임상시험이 2건이었다. 한국얀센이 허가받은 임상시험은 약 4건으로 JNJ-61186372 임상시험이 2건, JNJ-89862175 임상시험과 JNJ-95437446 임상시험이 각각 1건씩 승인받았다. 그 중에서도 JNJ-61186372는 ▲전이성 비소세포폐암에서 아미반타맙+올로모라십 병용요법 ▲절제 불가능 전이성 비소세포폐암에서 아미반타맙+카프마티닙 병용요법의 안전성과 유효성을 평가하는 임상시험으로 승인받았다. 2상이상 3상미만의 단계에서는 한국애브비가 승인받은 임상시험이 4건으로 가장 많았다. 이 중 ABBV-400(텔리소투주맙) 임상시험은 총 2건이 승인된 가운데 ▲MET 증폭이 있는 국소 진
- 노영희 기자
- 2026-01-06 06:00
-
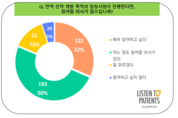
국내 환자·보호자 10명 중 8명, “신약개발 임상시험 참여 의향 있다”
한국환자단체연합회(대표 안기종)와 리슨투페이션츠(대표 명성옥)가 공동주최로 환자 및 보호자들의 임상시험 참여에 대한 인식 변화 설문조사를 11월 18일부터 12월 2일까지 2주간 실시, 그 결과를 발표했다. 이번 조사는 환자와 보호자들이 신약개발을 위한 임상시험에 대해 어떤 태도와 기대를 가지고 있는지, 참여 또는 비참여의 구체적 이유는 무엇인지, 과거와 비교했을 때 임상시험 참여의지에 대한 인식 변화가 있었는지를 알아보기 위해 마련됐다. 본 조사에 참여한 응답자는 총 387명(환자 229명, 보호자 158명)으로, 참여자 중 암 환자·보호자군이 136명, 희귀·중증난치질환 환자·보호자군이 107명, 기타 질환 환자·보호자군이 144명이었다. 설문에 따르면, ‘신약개발 목적의 임상시험이 진행된다면 참여할 의사가 있는가’라는 질문에 대해 △매우 참여하고 싶다/122명(32%), △어느 정도 참여할 의사가 있다/193명(50%)로 응답해 전체 응답자 387명 중 315명(82%)이 ‘참여 의향이 있다’고 답했다. 임상시험 참여 의향이 있는 이유를 묻는 설문에는△현재 치료의 효과 부족 또는 부작용으로 새로운 치료기회를 얻고 싶어서/166명 △신약개발 및 의학 발전
- 노영희 기자
- 2025-12-09 08:58
-
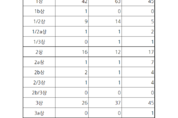
3분기 주요 제약바이오사 임상 135건 승인…노바티스 선두
식약처 의약품안전나라 사이트를 통해 3분기 주요 제약바이오사의 임상시험 승인 현황이 확인된 가운데 비교적 3상 이상 단계에서 많은 임상시험 승인이 이뤄진 것으로 나타났다. 3분기 주요 제약바이오사가 승인받은 임상시험은 약 135건으로, 이 중 1상 이상 2상 미만의 단계에서는 53건이 승인됐다. 특히 1상 이상 2상 미만의 단계에서는 아스트라제네카가 4건으로 가장 많은 임상시험이 승인됐다. AZD5335는 고형암 환자를 대상으로 한 단일요법으로서 및 다른 항암제와의 병용요법으로서 증량을 통해 연구될 예정이다. AZD4512는 두 건의 임상시험을 승인받았다. 이에 따라 ▲재발성/불응성 B-세포 비-호지킨 림프종(B-NHL) 시험대상자에서 단일요법 또는 다른 항암제와 병용요법 ▲급성 림프 모구성 백혈병 시험대상자에서 단일요법 또는 항암제와 병용요법으로 연구될 예정이다. STEAP2, CD3, CD8을 표적으로 하는 T 세포 관여 항체 AZD6621는 전이성 전립선암이 있는 성인환자를 대상으로 연구된다. 2상 이상 3상 미만은 총 32건이 승인됐다. 이 단계에서는 노바티스와 애브비가 승인받은 임상시험 건수가 각 4건으로 가장 많았다. 노바티스가 승인받은 임상시험
- 노영희 기자
- 2025-10-02 05:54
-

서울아산병원, 1분기 임상 8건 승인…주요 병원 중 최다
식품의약품안전처 의약품 안전나라를 통해서 병원 및 연구회가 2025년 1분기에 의뢰한 임상시험이 총 33건인 것으로 나타난 가운데 이 중가장 많은 임상시험을 의뢰한 기관은 8건을 의뢰한 서울아산병원으로 확인됐다. 서울아산병원이 의뢰한 8건의 임상시험을 살펴보면 1/2상으로는 위암 치료를 위한 빌로이, 다발골수종 치료를 위한 텍베일리관련 임상시험이 승인됐다. 2상에서는 신경내분비암 환자 대상 임상시험인 탈라타맙과 요통환자 진통주사인 VVZ-149HCI에 대한 연구를 승인받았고, 3상에서는식도암 환자 대상 보조항암요법을, 4상에서는 크론병 환자 대상으로 우스테키누맙의 치료 효능을 평가하는임상시험이 승인됐다. 연구자 임상시험으로는 특발성 폐섬유화증 환자 치료를 위한 펙수프라잔, 기립성불내성 환자에서의 어지럼증 완화 및 뇌혈류 개선 등을 평가하는 기넥신 연구가 승인됐다. 아산병원 다음으로 임상시험 승인을 많이 받은 세브란스병원은 총 6건의임상을 올 1분기 승인받았다. 간세포암 근치적 절제술 후개발 예방 효과를 연구하는 2상 임상시험을 제외하면 모두 연구자 임상시험이었다. 연구자 임상시험으로 승인받은 임상시험 적응증으로는 만성 척수손상, 베체트장염, 투명세포
- 노영희 기자
- 2025-04-02 05:35
-

1분기 주요 제약바이오사 임상시험 100건 승인
식품의약품안전처 의약품안전나라에 따르면 2025년 1분기 주요 제약바이오사는 100여건의 임상시험을 승인받은 것으로 나타났다. 세부적으로는 1상이상 2상미만이 53건, 2상이상 3상미만은 26건, 3상이상은 27건으로 확인됐다. 1상이상 2상미만 단계에서는 유한양행 자회사인 애드파마가 5건으로 가장 많았다. 내용을 살펴보면 AD-120, AD-115A, AD-227, AD-113, AD-228 등에 대한 임상시험이 승인받았다. 베이진코리아에서도 올 1분기 1상 단계에서 4건의 임상시험을 승인받았다. 대표적으로 BG-60366는 EGFR-돌연변이 비소세포 폐암 환자를 대상으로 EGFR 분해 CDAC인 BG-60366의 안전성, 내약성 등에 대해 연구하는 임상시험으로 승인받았다. 또 BGB-58067는 진행성 고형 종양 환자를 대상으로 한 MTA-협력 PRMT5 억제제 ‘BGB-58067’의 안전성 등을 조사하는 임상시험으로 승인됐다. 이외에도 BG-68501/BGB-43395, BG-C137에 대한 임상시험이 승인됐다. 2상 이상의 임상시험에서는 한국MSD가 3건을 승인받으며 가장 많이 승인받은 것으로 확인됐다. Sotatercept /MK-7962 (ACE-
- 노영희 기자
- 2025-04-01 06:00
-

4분기 임상 침체 속 희귀∙중증질환 3상 승인에 기대감↑
지난 해 4분기 임상시험 승인 건수는 비교적 저조했지만 결장직장암, 화농성한선염, 월경편두통 예방, 골수섬유증 등 다양한 적응증의 치료제들이 임상3상 단계에 접어들며 새 약물 탄생을 예고하고 있다. 의약품 안전나라에 따르면 2024년 4분기 주요 제약바이오사가 식품의약품안전처로부터 승인받은 임상시험은 약 98건으로 100건에 못미치는 모습이었다. 1상 이상 2상 미만이 56건, 2상 이상 3상 미만이 19건, 3상 이상이 23건이었다. 작년 전체로만 보면 주요 제약바이오사는 총 487건의 임상시험을 승인받았는데, 1상 이상 2상 미만은 265건, 2상 이상 3상 미만이 79건, 3상 이상이 143건이었다. 2024년 4분기 1상 이상 2상 미만 단계에서는 보령이 8건으로 가장 많은 임상시험을 승인받았다. BR7402에 대한 임상시험이 1건, VR1018에 대한 임상시험이 1건, BR1015에 대한 임상시험이 4건, BR1017에 대한 임상시험이 2건이었다. 보령 다음으로는 종근당이 승인받은 임상시험 건수가 가장 많았는데, CKD-324에 대한 임상시험이 1건, CKD-383에 대한 임상시험이 2건, CKD-379에 대한 임상시험이 1건, CKD-378에 대한
- 노영희 기자
- 2025-01-06 05:55
-
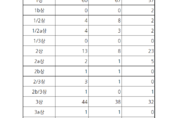
3분기, 2상단계 임상승인↑…항암제 연구 승인 多
많은 항암제들이 올 3분기 임상시험을 승인받으면서 새로운 치료방법 등장에 대한 기대감을 모으고 있다. 2024년 3분기 주요 제약바이오사의 임상시험 승인 현황을 확인한 결과, 약 125건의 임상시험이 승인된 것으로 나타났다. 올해 1, 2분기와 큰 차이는 없었지만 이번 3분기에는 특히 임상2상 단계 승인 건수가 전분기들 대비 많은 모습이었다. 1상이상 2상미만 단계에서는 약 63건의 임상시험이 승인됐다. 특히 이 단계에서는 보령이 5건으로 가장 많은 임상시험을 승인받았다. 승인 대상 약물은 BR5002, BR1400, BR1019, BR3409(2건)이었다. 대표적으로 BR5002는 건강한 성인 자원자를 대상으로 ‘BR5002-3’과 ‘BR5002-2’의 약동학과 안전성을 비교∙평가하기 위한 임상시험을, BR1400은 건강한 성인 자원자를 대상으로 ‘BR1400-1’, ‘BR1400-2’, ‘BR1400-3’ 투여 시의 용량별 약동학적, 약력학적 특성과 안전성을 비교∙평가하기 위한 임상시험을 승인받았다. 다국적제약사 중에서는 베이진코리아가 2건의 임상시험을 승인받았다. 임상시험을 승인받은 약물 중 BGB-43395는 전이성 HR+/HER2- 유방암 및 기타
- 노영희 기자
- 2024-10-04 05:40
-
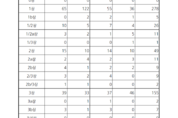
4분기 ‘3상’ 임상승인 최다…출시 기대 약물은?
2023년 4분기 제약바이오사의 임상시험 승인 건수가 올해 최저로 나타난 가운데, 3상 승인 건수는 올해 제일 많은 것으로 나타나 의미있는 한 해를 마무리했다. 식품의약품안전처의 의약품안전나라에 따르면 주요 제약바이오사의 2023년 4분기 1상 이상 2상 미만 승인은 47건, 2상 이상 3상 미만 승인은 15건, 3상 이상 4상 미만 승인은 46건, 연장 단계가 1건으로 총 109건의 임상시험을 승인받은 것이 확인됐다. 1상 이상 2상 미만 단계에서 가장 많은 임상시험을 승인받은 제약사는 보령으로 총 8건의 임상시험을 허가받았다. 세부적으로는 BR3005가 2건, BR3006가 2건이었으며 BR1019, BR1017-1, BR5002, BR5001이 각각 한 건씩 허가를 받았다. 대표적으로 BR3005의 임상시험은 건강한 성인 자원자를 대상으로 BR3005 복합제 단독 투여 시와 ‘BR3005-1’ 및 ‘BR3005-2’ 단일제 병용투여 시 약동학과 안전성을 비교 평가하기 위한 임상시험으로, 각각 공복 및 식후의 조건에서 한 건씩 진행된다. 한국아스트라제네카도 5건의 임상시험을 승인받았다. 절제 불가능한 국소 진행 또는 전이된 호르몬 수용체 양성(HR+),
- 노영희 기자
- 2024-01-02 05:40
-

더웨이헬스케어-세이프소프트, 임상 플랫폼 사업 MOU 체결
㈜더웨이헬스케어가 임상시험 실무 플랫폼의 고도화 작업 및 내부 효율화를 높이기 위해 ㈜세이프소프트와 손을 잡았다. 헬스케어 시장에서 임상과 마케팅 서비스를 제공하는 전문 종합대행사 ㈜더웨이헬스케어(대표 이정우)가 소프트웨어 개발 및 인증, 검증 전문기업 ㈜세이프소프트(대표 이동훈)가 지난 11월 9일 ㈜세이프소프트 본사에서 전략적 업무협약을 체결하고 본격적인 행보에 들어갔다고 밝혔다. ㈜더웨이헬스케어와 업무협약을 체결한㈜세이프소프트는 국내 최대 기업군인 Dt&C Healthcare Group 내 계열사들의 임상수행 경험과 지식정보, 최신의 기술 그리고 아이디어를 통해 최적화된 E-임상솔루션을 개발하고 있다. 비임상시험에서부터 의약품/의료기기/건강기능성식품 등 임상시험, 허가까지의 전 영역을 다룰 수 있는국내 유일의 E-임상 Total solution을 보유한 기업이다. ㈜더웨이헬스케어는 임상시험 시장에서 쌓은 노하우를 바탕으로, 원격 임상시험 통합 관리 서비스플랫폼인, ‘아이크로 패밀리’를 출시한 바 있다. ‘아이크로 패밀리’는 비용 절감과 편의성, 프로세스 개선 효과를 제공하는 임상 시험 실무 플랫폼이다.이번 업무협약을 통해 ‘아이크로 패밀리’의 고
- 노영희 기자
- 2023-11-13 13:24
-
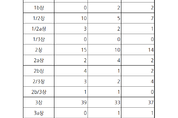
3분기 임상승인 129건 중 과반이 1상에…어떤 약물 탄생될까
2023년 3분기 제약·바이오사가 승인받은 임상시험의 과반 이상이 1상이상 2상미만 단계에 있는 것으로 확인되면서 다양한 약물의 등장 가능성을 보이고 있다. 식품의약품안전처의 의약품 안전나라를 통해서 2023년 3분기 주요 제약바이오회사들의 임상시험 승인 건수가 총 129건으로 확인됐다. 이 중 129건 중 1상이상 2상미만이 65건, 2상이상 3상미만이 22건, 3상이상이 42건으로 주로 임상 진입 초기단계에서 높은 실적을 보였다. ◆1상이상 2상 미만, ‘대원제약’이 5건으로 최다 새 약물 개발을 위한 다양한 제약사들의 도전이 이뤄지고 있는 가운데, 이 단계에서는 대원제약이 5건으로 가장 많은 임상시험을 승인받았다. 세부적으로는 DW1122에 관한 임상 4건과 DW1021에 관한 임상 1건이었다. ‘DW1122’ 임상 중 2건은 건강한 성인 자원자를 대상으로 DW1122-T2와 각 단일제인 DW1122-R2와 DW1122-R3의 병용투여 시 식전 또는 식후에서의 안전성과 약동학적 특성을 비교 평가하기 위한 연구로 승인됐다. 또 건강한 성인 자원자를 대상으로 DW1122-T1과 각 단일제인 DW1122-R1과 DW1122-R2의 병용투여 시 식전 또는 식후
- 노영희 기자
- 2023-10-04 05:40
- [동정]병협 첫 여성회장 탄생…유경하 이대의료원장 당선
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]순천향대 부천병원 문종호 교수, ‘제19대 대한췌장담도학회 이사장’ 취임
- [인사]SK바이오, R&D 실행력 강화 위해 연구지원조직 정비 및 핵심인재 영입
- [인사]화순전남대병원 김인영 교수, 대한정위기능신경외과학회장 선임
- [인사]원광대병원 김정우 교수, 대한견주관절학회 제34대 회장 취임
- [인사]일동제약그룹 정기승진인사 (4/1)
- [인사]한국산텐제약, 신임 대표이사에 김진희 대표 선임 (4/1)
- [인사]일동제약, 새 R&D 본부장 박재홍 사장 선임
- [동정]병협 첫 여성회장 탄생…유경하 이대의료원장 당선
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [동정]가정의학과의사회 유승호 공보이사, 보건복지부 장관상 수상
- [동정]경북대병원 김혜정 연구교수·박준석 교수 연구팀, 대한대장항문학회 ‘우수포스터상’ 수상













