-

셀트리온, 아일리아 바이오시밀러 CT-P42 유럽 품목허가 신청
셀트리온이 현지 시간 23일 유럽의약품청(EMA)에 아일리아(EYLEA, 성분명: 애플리버셉트) 바이오시밀러 CT-P42의 품목허가 신청을 완료했다. 셀트리온은 아일리아가 유럽에서 보유한 습성 황반변성(wAMD), 망막정맥 폐쇄성(CRVO·BRVO) 황반부종, 당뇨병성 황반부종(DME), 근시성 맥락막 신생혈관(CNV) 적응증에 대해 품목허가를 신청했다. 이번 허가 신청은 CT-P42의 글로벌 임상 3상 결과를 바탕으로 이뤄졌다. 셀트리온은 체코, 헝가리, 폴란드, 스페인 등 총 13개국에서 당뇨병성 황반부종 환자 348명을 대상으로 진행된 임상 3상을 통해 오리지널 의약품 대비 동등성 및 유사성을 확인한 바 있다. CT-P42의 오리지널 의약품인 아일리아는 지난해 전세계에서 약 97억 5,699만 달러(약 12조 6,841억원)의 매출을 기록했다. 아일리아의 미국 독점권은 2024년 5월, 유럽 물질특허는 2025년 11월 만료될 예정이다. 셀트리온 관계자는 “CT-P42의 글로벌 임상 3상 결과를 바탕으로 미국, 한국, 유럽 등 주요국에 순차적으로 품목허가 신청을 완료하고 글로벌 시장 진출을 순조롭게 준비 중”이라며 “기존 강점을 보이던 자가면역질환과 항
- 노영희 기자
- 2023-11-24 13:01
-
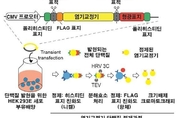
선천망막질환, 바이러스 대신 단백질로 유전자 교정
서울대병원 안과 김정훈 교수팀(고려대학교 우재성 교수·한양대학교 배상수 교수)은 선천망막질환 치료에 적합한 염기교정기 리보핵산단백질 합성 기술을 개발했다. 선천망막질환은 유전자 돌연변이로 발생하며, 소아 실명의 주요 원인이다. 전 세계 약 200만 명이 앓고 있는 것으로 알려져 있으며, 치료법으로는 유전자를 염기 단위로 제거하거나 교체하는 유전자가위 기술이 널리 연구 중이다. 최근에는 DNA를 절단하지 않아 부작용이 적은 염기교정기 방식이 주목받고 있다. 연구팀은 태아 세포주 HEK293E에서 국제 표준에 적합한 순도 99% 이상의 염기교정기 리보핵산단백질을 확보했다. 이후 rd12 생쥐에게 해당 단백질을 투여해 우수한 치료 효과를 확인했다. rd12는 정상적인 RPE65 단백질을 생성하지 못해 선천망막질환을 앓는 생쥐 모델이다. 확보한 염기교정기 리보핵산단백질을 생쥐에게 투여했을 때, 정상적인 DNA 교정과 RPE65 단백질 발현을 확인했다. 연구팀이 개발한 염기교정기 단백질 합성 기술은 기존에 널리 사용되는 바이러스 방식보다 안정성, 속도, 비용 측면에서 모두 우수한 것으로 나타났다. 먼저 안정성 측면에서 부작용이 적다. 단백질 방식은 플라스미드를 이용한
- 신대현 기자
- 2021-09-09 10:47
- [인사]한국페링제약, 김민정 신임 대표 선임 (5/1)
- [인사]휴온스메디텍, 이진석 신임 대표 선임
- [인사]전북대병원 조용곤 교수, 전북대병원 의생명연구원장 취임
- [인사]한국원자력의학원 인사(5/8)
- [인사]아주대병원 원제환 교수 아·태 인터벤션 영상의학회 회장 선출
- [인사]보건복지부 인사(5/9~10)
- [인사]전남대병원 김병채 교수, 대한치매학회 회장 선출
- [인사]한승범 고대 안암병원장, 상급종합병원협의회 신임회장 취임
- [인사]고신대복음병원, 최종순 교수를 신임 병원장으로 선임
- [인사]한국로슈, 에잣 아젬 대표이사 선임 (5/1)
- [동정]고대 구로병원, 박일호 교수팀, 규제혁신 로봇실증사업 선정
- [동정]고대 구로병원 이영선 교수팀, 전사인자 기반 염증 혁신 약물 개발 추진
- [동정]창원경상대병원 안효정 교수팀, miR-127-3p 암전이 촉진 논문 발표
- [동정]충남대병원 응급의학과 의료진, 국제학술지에 논문 게재
- [동정]서울아산병원 이중선 교수, 스마트 웨어러블기기 활용 정신건강 모니터링 플랫폼 개발 착수
- [동정]고대 구로병원 조금준 교수팀, 과기부 ‘STEAM 연구사업’ 선정
- [동정]종근당건강, 2024 iF 디자인 어워드 ‘디자인상’ 수상
- [동정]한림대 동탄성심병원 송시영 교수, 무릎 인공관절치환술 수명 향상 국책 연구과제 선정
- [동정]엔비피헬스케어 ‘SCI평가정보 기술평가 우수기업 인증 T3’ 획득
- [동정]충남대병원 우성대·박희선 교수, 알레르기 분야 국제학술지에 논문 게재















