4년간 전세계 세포·유전자 치료제 임상 32%↑..북미 가장 활발
미국 재생의료연구연합회, 보고서 발간
- 양민후 기자 minhuy@medifonews.com
- 등록 2019-11-04 05:50:00
지난 4년간 전세계 첨단바이오의약품(ATMP) 관련 신규 임상시험이 약 32% 증가한 것으로 나타났다. 임상연구가 가장 활발히 이뤄진 대륙은 북미였다. 아시아는 2위, 유럽은 3위를 기록했다. 벨기에는 규모에 비해 매력적인 임상시험 사이트 역할을 수행한 것으로 평가됐다. ATMP 개발과 관련, 우호적인 환경을 제공한 것이 유효하게 작용했다.
미국 재생의료연구연합회(ARM)는 최근 이 같은 내용의 보고서를 발간했다.
이에 따르면, 전세계 세포·유전자치료제
등
ATMP 관련 신규 임상시험은 2014년 318건에서 2018년 424건으로
약 32% 증가했다.
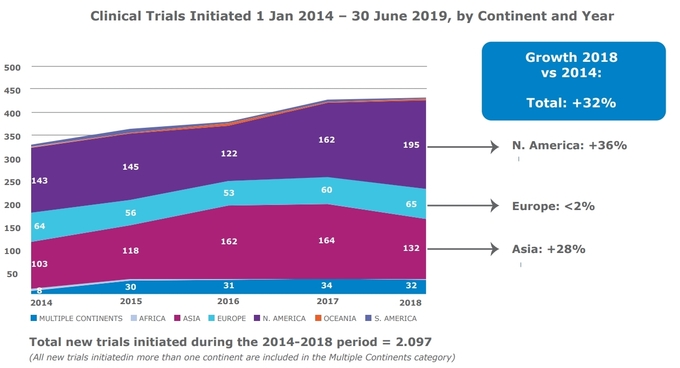
가장 두드러진 성장세를 보인 대륙은 북미였다. 2014년 143건에서 2018년 195건으로
36% 늘었다. 아시아는 뒤를 이었다. 지난 4년간 103건에서
132건으로 28% 성장했다. 반면 유럽은 2014년 64건, 2015년 56건, 2016년
53건, 2017년 60건, 그리고 2018년 65건으로 매년 비슷한 수준을 유지했다.
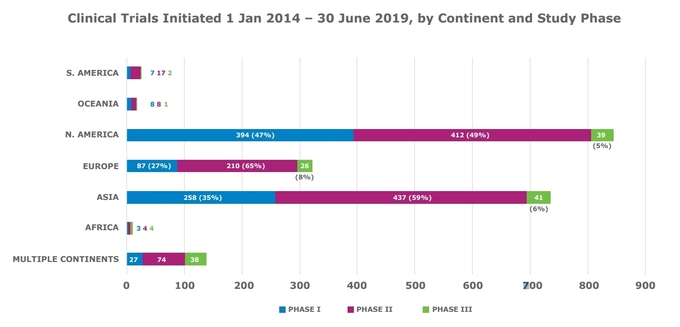
북미는 1상 임상시험 비율이 가장 높았다. 2014년부터 2019년 6월 사이 개시한 ATMP 임상시험 845건 중 394건(47%)이 1상 단계였다. 같은 기간 아시아에서 258건(35%), 유럽에서 87건(27%)의 1상 임상시험이 보고됐다.
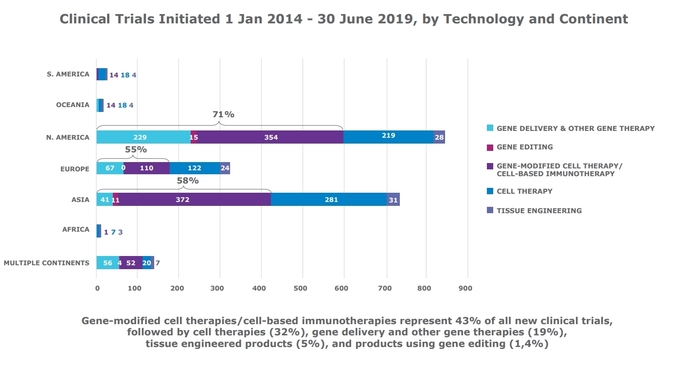
새로운 시도 역시 북미에서 가장 많이 이뤄졌다. 845건 중 598건(71%)이 유전자 전달, 편집, 변형 등을 기반으로 한 치료제 관련 임상시험이었다. 이런
시도는 아시아에서 424건, 유럽에서 177건 확인됐다.
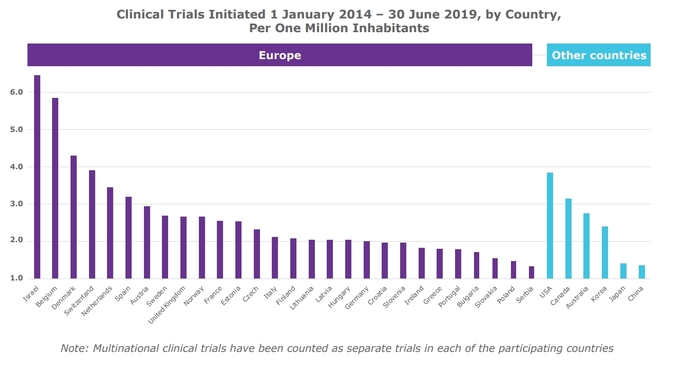
이와 함께 일부 유럽국가는 오히려 북미보다 매력적인 임상시험 사이트 역할을 수행한 것으로 나타났다. ATMP 임상시험 수를 1인당(per capita)으로 살펴본 결과, 이스라엘·벨기에·덴마크 등은 미국·캐나다보다 우수한 지표를 보였다. 반대로 독일 등은 저조한 기록을 남겼다.
기업들은 임상시험 허가 결정이 빠른 나라에 매력을 느꼈다. 벨기에의 경우 임상시험 승인에 평균 30~60일 걸린 것으로 조사됐다. 반면 독일은 같은 결정에 6~12개월을 소요했다.
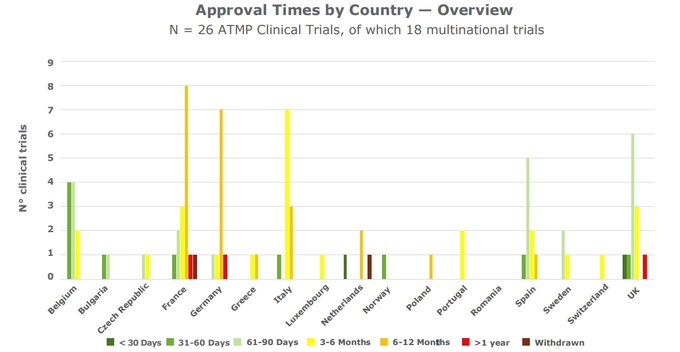
전반적으로 유럽은 여러 지표에서 북미에 뒤쳐졌다. 이는 ATMP 임상시험 허가과정의 복잡성에 따른 것으로 풀이된다. 일례로 EU는 유전자치료제를 GMO(유전자변형생물)로 분류하면서 임상시험 개시까지 추가적인 절차를 요구하고 있다.
EU는 ATMP 임상시험 신청 과정을 보다 단순화할 예정이다. 2020년까지 'Clinical Trial Regulation' 법안 적용을 계획하고 있다. 다만 해당 법안은 임상시험 허가결정 신속화 등의 내용을 담고 있지는 않다.
- [인사]대원제약 정기 승진 인사 (3/1)
- [동정]여의도성모병원 윤혜연 교수, 한국각막학회 국제학술대회 ‘Best Presentation Award’ 수상
- [동정]고대구로병원 이승룡 교수, '제19회 암 예방의날' 행사서 ‘국무총리 표창’ 수상
- [인사]CSL, 한국 법인에 황세은 신임 대표 선임
- [동정]부천성모병원 지희정 간호사, ‘암 예방의 날’ 보건복지부 장관 표창 수상
- [동정]휴온스, 성남상공대상서 ‘ESG경영대상’ 수상
- [동정]김상진 대한가정의학과의사회 의무이사, 보건복지부 장관표창 수상
- [동정]고대 안산병원 민경진 교수, ‘제19회 암 예방의 날 기념식’ 보건복지부장관 표창
- [동정]충남대학교병원 박수용 교수, 대한진단혈액학회 학술대회 최우수 구연상
- [동정]제19회 암예방의 날, 국립암센터 이건국 연구소장 ‘국민포장’, 최정미 사무국장 ‘국무총리 표창’ 수상
- [인사]대원제약 정기 승진 인사 (3/1)
- [인사]CSL, 한국 법인에 황세은 신임 대표 선임
- [인사]충북대병원 최미영 교수, 제18대 한국사시소아안과학회 회장 선출
- [인사]질병관리청 공무원 과장급 전보 (3/16)
- [인사]식약처 국·과장급 인사발령 (3/16)
- [인사]강동경희대학교병원 김동환 교수, 대한암재활학회 차기 회장 선출
- [인사]경희대학교병원 백종우 교수, 한국자살예방협회 회장 취임
- [인사]단국대병원 박재석 교수, 대한결핵 및 호흡기학회 회장 취임
- [인사]원텍, 영업총괄·권역별 법인장·연구소장 인사 단행
- [인사]질병관리청 승진 및 전보 (3/9)
- [동정]여의도성모병원 윤혜연 교수, 한국각막학회 국제학술대회 ‘Best Presentation Award’ 수상
- [동정]고대구로병원 이승룡 교수, '제19회 암 예방의날' 행사서 ‘국무총리 표창’ 수상
- [동정]부천성모병원 지희정 간호사, ‘암 예방의 날’ 보건복지부 장관 표창 수상
- [동정]휴온스, 성남상공대상서 ‘ESG경영대상’ 수상
- [동정]김상진 대한가정의학과의사회 의무이사, 보건복지부 장관표창 수상
- [동정]고대 안산병원 민경진 교수, ‘제19회 암 예방의 날 기념식’ 보건복지부장관 표창
- [동정]충남대학교병원 박수용 교수, 대한진단혈액학회 학술대회 최우수 구연상
- [동정]제19회 암예방의 날, 국립암센터 이건국 연구소장 ‘국민포장’, 최정미 사무국장 ‘국무총리 표창’ 수상
- [동정]가천대 길병원 이기택 교수, 암예방의 날 대통령 표창
- [동정]제주대학교병원 홍지수 간호사, ‘제6회 미래선도 간호사상’ 수상













