화이자, '프리베나13' 뛰어넘을 20가 백신 향한 항해 시작
FDA 혁신치료제 지정 20가 폐렴구균 접합 백신 3상 임상 개시
- 김윤미 기자 kym@medifonews.com
- 등록 2018-12-17 05:40:00
화이자가 자사의 13가 폐렴구균 접합백신 '프리베나13'의 후속작으로 개발 중인 20가 폐렴구균 접합백신 후보물질 ‘PF-06482077’의 3상 임상 프로그램을 개시했다.
 화이자는 18세 이상 성인을 대상으로 자사가 개발중인 20가 폐렴구균 결합백신(20vPnC) ‘PF-06482077’의 백신에 포함된 폐렴구균 혈청형에 의한 침습성 질환이나 폐렴 예방 효과를 평가하기 위한 3상 임상 프로그램을 개시했다고 14일(현지시각) 발표했다.
화이자는 18세 이상 성인을 대상으로 자사가 개발중인 20가 폐렴구균 결합백신(20vPnC) ‘PF-06482077’의 백신에 포함된 폐렴구균 혈청형에 의한 침습성 질환이나 폐렴 예방 효과를 평가하기 위한 3상 임상 프로그램을 개시했다고 14일(현지시각) 발표했다.
‘PF-06482077’은 화이자가 폐렴 백신 분야에서 '프리베나13' 후속작으로 개발 중인 후보물질로서, 지난 9월 20일 미 FDA로부터 18세 이상 성인에서 침습성 질환 및 폐렴 예방에 '혁신치료제(Breakthrough Therapy)' 지정을 받은 바 있다.
3상 연구는 총 3,880명의 성인이 참여하며, 60세 이상 성인에서 ‘PF-06482077’을 접종한 군과 13가 폐렴구균 접합백신과 23가 폐렴구균 다당류 백신을 접종한 대조군과의 면역 반응 비교, 18~59세 성인에서 ‘PF-06482077’의 면역원성 평가, 그리고 18세 이상 성인에서 ‘PF-06482077’의 안전성 프로파일을 정의하기 위해 진행된다.
화이자의 수석부사장이자 백신 연구개발 책임자인 캐서린 유 잰스(Kathrin U. Jansen) 박사는 "현재도 성인에서 프리베나13에 의한 전범위 보호가 실현되고는 있지만, 화이자는 우리가 개발중인 20가 백신이 아직 기존 백신에 포함되지 않은 혈청형으로 인한 상당한 침습적 질환이나 폐렴으로부터 성인을 보호하는 데 중요한 다음 단계가 될 것을 기대한다"고 전했다.
이어 그는 "화이자는 폐렴구균 접합 백신 업계의 선두주자로서, 지난 9월 FDA의 혁신치료제로 지정을 받은 3세대 폐렴구균 백신의 3상 임상시험을 시작하게 되어 자랑스럽게 생각한다"고 덧붙였다.
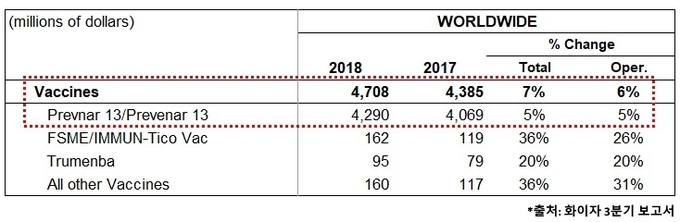
한편, 화이자 백신사업부의 글로벌 매출은 2018년 3분기까지 누계 약 47억 8백만 달러(5조 3,412억 원) 규모로, 이 중 '프리베나13'의 매출이 42억 9천만 달러(4조 8,670억 원) 규모로 백신사업부 전체 매출의 약 91% 이상을 차지하고 있다.
또한 '프리베나13'의 3분기까지의 누계 매출은 작년 동기 글로벌 매출인 43억 8,500만 달러 대비 5% 상승한 수치로, 유럽을 제외한 미국 등 대부분의 국가에서 상승세를 유지하고 있어, 이번 20가 백신의 3상 임상이 성공적으로 마무리될 경우 세대 교체에 따른 백신사업부의 확장 역시 기대된다.
- [동정]경희의료원보 ‘프러포즈’, 대한민국 커뮤니케이션 대상 수상
- [동정]국립중앙의료원 중앙응급의료센터, ‘2025 대한민국 커뮤니케이션대상’ 2개 부문 수상
- [동정]단국대병원 이정재 교수, 중소벤처기업부장관상 수상
- [동정]국립암센터 강미주 기획책임관, 대통령 표창 수상
- [동정]한국원자력의학원 김진수 책임연구원, 국회 보건복지위원장상 수상
- [동정]가천대 길병원 선우웅상 연구부원장, 보건복지부 장관 표창
- [동정]영남대학교병원, 2025년 한국의료질향상학회 가을학술대회 우수상 수상
- [동정]한림대춘천성심병원 박찬흠 교수팀, 우주항공청 '스페이스 해커톤 대회' 대상 수상
- [동정]아주대병원 노성현 교수팀, 대한척추신기술학회 ‘최우수구연상 수상’
- [인사]전남대병원 정신 교수, 대한뇌신경기능장애연구회 신임 회장 취임
- [인사]전남대병원 정신 교수, 대한뇌신경기능장애연구회 신임 회장 취임
- [인사]국립암센터 박현진 교수, 대한소아혈액종양학회 이사장 취임
- [인사]녹십자홀딩스, 박소영 전략기획실장 영입
- [인사]GC 계열사 정기임원인사 단행 (1/1)
- [인사]대한치주과학회 차기회장에 정조혁 現 부회장 선출
- [인사]삼성서울병원, 2026년 정기 임원인사(11/26)
- [인사]국립중앙의료원 홍수종 전문의, 아시아태평양 소아알레르기호흡기면역학회(APAPARI) 회장 취임
- [인사]고성규 경희대 한의과대학 학장, 국가신약개발재단 차기 이사장 선출
- [인사]전북대병원 양종철 병원장, 2027년 회기 대한신경정신의학회 학회장 선출
- [인사]대한통증학회 차기 회장에 박휴정 교수 선출
- [동정]경희의료원보 ‘프러포즈’, 대한민국 커뮤니케이션 대상 수상
- [동정]국립중앙의료원 중앙응급의료센터, ‘2025 대한민국 커뮤니케이션대상’ 2개 부문 수상
- [동정]단국대병원 이정재 교수, 중소벤처기업부장관상 수상
- [동정]국립암센터 강미주 기획책임관, 대통령 표창 수상
- [동정]한국원자력의학원 김진수 책임연구원, 국회 보건복지위원장상 수상
- [동정]가천대 길병원 선우웅상 연구부원장, 보건복지부 장관 표창
- [동정]영남대학교병원, 2025년 한국의료질향상학회 가을학술대회 우수상 수상
- [동정]한림대춘천성심병원 박찬흠 교수팀, 우주항공청 '스페이스 해커톤 대회' 대상 수상
- [동정]아주대병원 노성현 교수팀, 대한척추신기술학회 ‘최우수구연상 수상’
- [동정]전남대병원 김민철 교수, ‘생명 살리는 심장 연구’ 공로로 복지부 장관 표창