AZ '임핀지', 3기 폐암 치료에 새 가능성 제시
면역치료요법 최초로 3기 폐암치료에 OS 혜택 입증한 PACIFIC 연구결과 발표
- 김윤미 기자 kym@medifonews.com
- 등록 2018-09-27 05:40:00
아스트라제네카의 '임핀지'는 항암화학방사선요법 이후 질병이 진행되지 않은 절제 불가능한 3기 비소세포폐암 환자에서 유의미한 무진행생존율 개선을 입증한 PACIFIC 연구 결과를 토대로, 올해 2월 미 FDA로부터 면역치료제 최초로 승인 받은 바 있다.
아스트라제네카가 이번에는 동 연구에서 '임핀지'의 전체생존율을 개선한 결과를 발표하며, 그간 치료옵션이 부족했던 3기 폐암 치료에 새로운 패러다임을 열 가능성을 제시했다.
25일(현지시각) 아스트라제네카는 국제폐암연구협회(IASLC)가 23~26일 캐나다 토론토에서 개최한 제19차 국제폐암컨퍼런스(WCLC)에서 '임핀지(더발루맙)'의 3상 임상인 PACIFIC 연구에서의 전체생존율(OS) 결과를 발표했다.
연구 결과는 '임핀지'는 PD-L1 발현과 상관없이 표준치료법에 비해 1차 평가변수인 전체생존율을 유의미하게 개선하여, 사망위험을 32% 감소시킨 것으로 나타났다.
해당 PACIFIC 연구는 동시 항암화학방사선요법 이후 질병이 진행되지 않는 절제 불가능한 비소세포폐암(NSCLC) 3기 환자에서 '임핀지'가 위약과 비교해 무진행생존율(PFS)을 유의하게 연장시켰다는 사실을 입증한 바 있다.
이번에 발표된 내용은 두 번째 1차 평가변수인 전체생존율 개선 결과가 중점적으로 보고됐다.
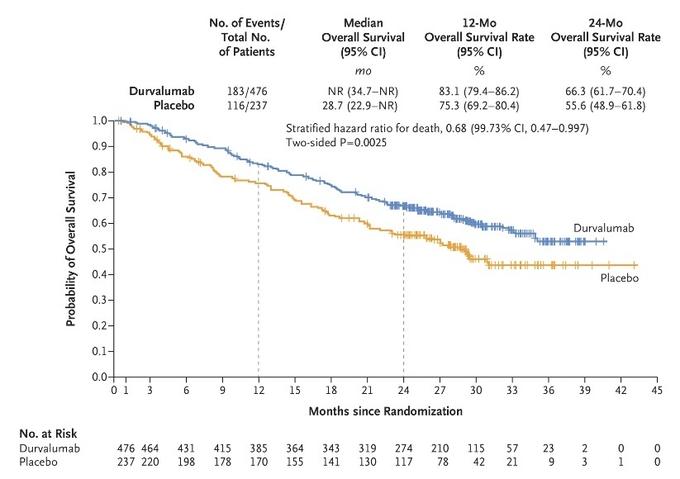
473명의 환자가 임핀지, 236명이 위약을 무작위 배정 받았으며, 2018년 3월 22일 기준으로 추적관찰 기간 중앙값은 25.2개월이었다. 24개월 전체생존율은 위약군에서 55.6%, 임핀지 군에서 66.3%로, 임핀지 군에서 전반적인 생존기간을 유의하게 연장시켰으며, 사망위험을 32% 감소시켰다(그림1).
무진행생존율에 대한 최신 분석 결과도 이전에 발표된 보고와 비슷했다. 무진행생존기간 중앙값은 임핀지 군에서 17.2개월, 위약군에서 5.6개월로 나타나 임핀지가 위약 대비 질병 진행 및 사망위험을 49% 감소키신 것으로 나타났다.
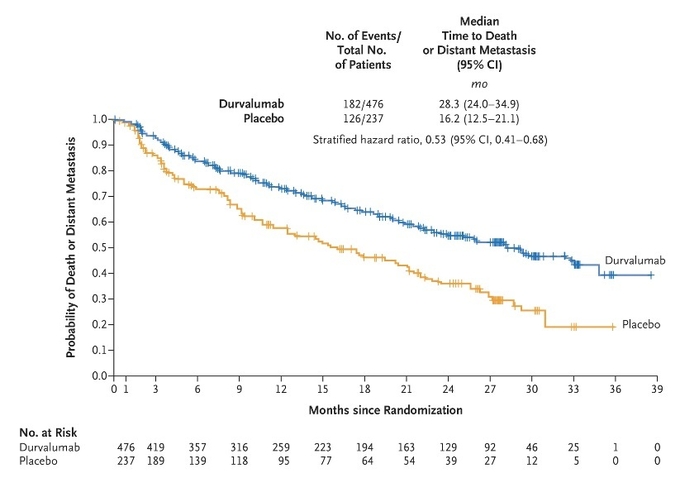
해당 연구의 2차 평가변수인 사망 또는 원격 전이까지 걸리는 시간의 중앙값은 임핀지 군에서 28.3개월, 위약군에서 16.2개월이었다(그림2).
임핀지 군의 30.5%와 위약군의 26.1%에서 3~4등급의 부작용이 발생했으며, 임핀지 군의 15.4%와 위약군의 9.8%는 부작용으로 인해 투약을 중단했다.
아스트라제네카 측은 "임핀지는 화학요법 치료 후 절제 불가능한 3기 비소세포폐암 환자의 전체생존율 혜택을 입증한 최초의 면역요법제로, 오늘의 발표는 지난 수십 년 동안 생존율에 개선이 없던 치료환경에서 환자들에게 새로운 희망을 가져다 줄 것"이라고 강조했다.
한편, 해당 연구 결과는 New England Journal of Medicine에서 'Overall Survival with Durvalumab after Chemoradiotherapy in Stage III NSCLC'란 제목으로 동시에 발표됐다.
- [인사]충북대학교병원 (2026년 1월 1일 자)
- [인사]서울성모병원 배자성 교수, 대한신경모니터링학회 회장 선임
- [동정]세종충남대병원 김선정 수간호사, 보건복지부 장관 표창
- [인사]브리츠메디, 이신재 신임 대표이사 취임 (12/2)
- [인사]보건복지부 인사 발령
- [인사]순천향대 부천병원 김기운 교수, ‘대한고압의학회 신임 이사장’ 선출
- [동정]한국원자력의학원 우상근 책임연구원, 국무총리 표창 수상
- [동정]경희대병원 박봉진·박창규 교수, 대한뇌신경기능장애연구회 우수연제상 수상
- [동정]대구가톨릭대학교병원, 공공보건의료 성과로 보건복지부 장관상 수상
- [동정]한림대성심병원, ‘급성심장정지조사 유공’ 보건복지부장관 표창
- [인사]충북대학교병원 (2026년 1월 1일 자)
- [인사]서울성모병원 배자성 교수, 대한신경모니터링학회 회장 선임
- [인사]브리츠메디, 이신재 신임 대표이사 취임 (12/2)
- [인사]보건복지부 인사 발령
- [인사]순천향대 부천병원 김기운 교수, ‘대한고압의학회 신임 이사장’ 선출
- [인사]순천향대 부천병원 이종대 교수, ‘대한안면신경학회 제5대 회장’ 선출
- [인사]휴온스그룹, 2026년 정기 임원 인사 실시 (1/1)
- [인사]고대 안암병원 이헌정 교수, 제3대 대한디지털치료학회장 선출
- [인사]노원을지대학교병원, 신임병원장에 김재훈 교수 선임
- [인사]보령 임원승진인사 단행…“전문성 중심 인재 중용”
- [동정]세종충남대병원 김선정 수간호사, 보건복지부 장관 표창
- [동정]한국원자력의학원 우상근 책임연구원, 국무총리 표창 수상
- [동정]경희대병원 박봉진·박창규 교수, 대한뇌신경기능장애연구회 우수연제상 수상
- [동정]대구가톨릭대학교병원, 공공보건의료 성과로 보건복지부 장관상 수상
- [동정]한림대성심병원, ‘급성심장정지조사 유공’ 보건복지부장관 표창
- [동정]건양대병원, 의료관련감염병 대응 유공 질병관리청장 표창
- [동정]멀츠 에스테틱스, 2025 지속가능개발목표경영지수 최우수그룹 선정
- [동정]연세의대 이정윤 교수, 2026 제7회 난소암 컨센서스 컨퍼런스 공동의장 선임
- [동정]원주의과대학 이승현 연구원, 한국보건정보통계학회 학술대회 우수상
- [동정]경희대병원 유명철 교수, 대한안면신경학회 최우수상 수상













