한국릴리, 3상이상 단계서 12건으로 최다 승인
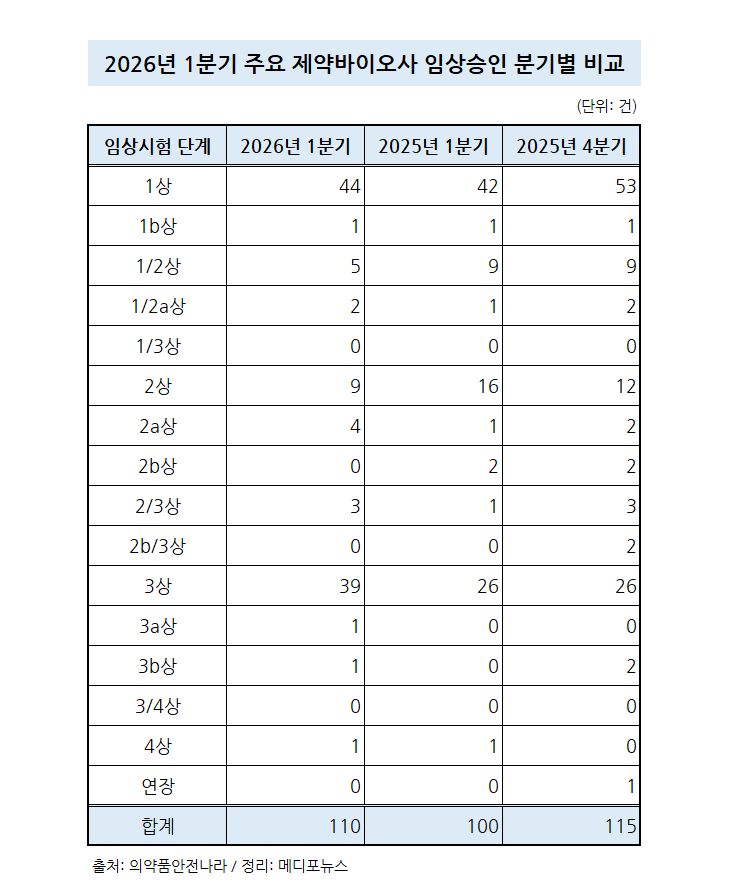
2026년 1분기 주요 제약바이오사가 총 110건의 임상시험을 승인받은 가운데, 3상이상 단계 승인이 3분의 1 이상을 차지한 것으로 나타났다.
식품의약품안전처 의약품안전나라를 통해 올 1분기 임상시험 승인 현황이
확인됐다.
먼저 1상이상 2상미만
단계에서는 52건이 승인됐는데 유한양행 자회사인 애드파마가 8건으로
가장 많이 임상시험을 승인받았다. 승인받은 약물은 AD-123, AD-229,
AD-118, AD-116, AD-229, AD-115A, AD-117 등이었는데, 대표적으로
AD-123은 건강한 성인 자원자를 대상으로 공복상태에서
AD-1231 및 AD-1232의 병용투여와 AD-123의
단독투여시 안전성과 약동학을 비교∙평가하기 위한 연구로 승인받았다.
보령에서도 5건의 임상시험을 승인받았는데 이 중 BR1015-A 임상시험만 4건이었다.
BR1015-A의 임상시험으로는 건강한 성인 자원자를 대상으로 BR1018-A 단독투여와
BR1018-1 및 BR1018-2 병용투여 시 약동학과
안전성을 비교∙평가하는 임상시험 등이 있다.
2상이상 3상미만 단계에서는 16건의 임상시험 승인이 이뤄졌다.
주요 승인현황을 보면 BMS의 푸미타미그에 대한 2건의 임상시험이 승인됐다. 이에 따라 ▲이전에 치료받지 않은 절제
불가능 또는 전이성 결장직장암 시험대상자에서 항암화학요법과 병용한 푸미타미그 대 항암화학요법과 병용한 베바시주맙에 대한 연구 ▲이전에 치료받지
않은 진행성 또는 전이성 위, 위식도 접합부 또는 식도 선암종이 있는 시험대상자에서 항암화학요법과 병용한
푸미타미그 대 항암화학요법과 병용한 니볼루맙에 대한 연구가 진행될 예정이다.
한미약품은 HM95573의 임상을 승인받아 NRAS돌연변이가 있는 국소 진행성 또는 전이성 흑색종 환자를 대상으로
Belvarafenib (HM95573)과 Cobimetinib의 병용요법을 평가하기 위한
임상시험 참여자를 모집 중이다.
한국노바티스는 애시미닙에 대해서 ▲알려진 T315I 돌연변이가 있거나
없는 만성기의 필라델피아 양성 만성 골수성 백혈병 (Ph+ CML-CP)으로 새로 진단되거나 이전에
치료받은 소아 참가자에서 애시미닙의 안전성 및 유효성을 평가하는 연구를 승인받았다.
3상 이상 단계에선 42건의
임상시험이 승인됐다.
이 단계에서는 릴리가 12건으로 가장 많이 승인을 받았다. 이 중 LY3841136가 4건의
승인을 받았는데 ▲무릎 골관절염 통증이 있는 비만 또는 과체중 성인 ▲제2형 당뇨병을 동반하지 않는 비만 또는 과체중 성인 ▲중등도 내지 중증의
폐쇄성 수면 무호흡증이 있는 비만 또는 과체중 성인 ▲제 2형
당뇨병을 동반한 비만 또는 과체중 성인 등을 대상으로 연구가 진행될 예정이다.
사노피는 5건의 승인을 이뤄낸 가운데 4건은 ‘Duvakitug’ 연구다.
중등증 내지 중증의 활동성 크론병 연구와 중등증 내지 중증의 활동성 궤양성 대장염 연구가 각각 2건이었다. 나머지 한 건인 Itepekimab 연구에서는 EFC18418 또는 EFC18419 임상시험에 참여한 적절히 조절되지
않는 비용종을 동반한 만성 비부비동염이 있는 성인 시험대상자를 대상으로 이테페키맙의 장기 안전성 및 내약성을 평가하게 된다.
MSD도 5건의 임상이
승인됐다. 이 중 MK-1084는 ▲국소적으로
병기가 진행됐고 절제가 이뤄지지 않은 KRAS G12C 돌연변이형 비소세포폐암을 앓고 있고 근치적 백금제제
기반 화학방사선요법 이후에 질병진행을 경험하지 않은 환자 ▲제IIA~IIIB(N2)기 KRAS G12C 돌연변이형 비소세포 폐암에
대해 완전 절제술을 받은 참가자를 대상으로 연구가 승인됐다.
1분기 제약바이오사가 승인받은 유일한 4상 임상은 고려제약의 ‘큐업액’ 연구다. 육체 피로가 있는 자를 대상으로 하는 큐업액의 유효성 및 안전성을 평가하기 위한 연구가 승인됐다.
노영희 기자 nyh2152@medifonews.com
< 저작권자 © Medifonews , 무단전재 및 재배포금지 >
- 본 기사내용의 모든 저작권은 메디포뉴스에 있습니다.
