소아 스테로이드 불응성/반응성 신증후군 환자 관련 다기관-무작위 배정 연구 3건 포함
국내 의료기관들 중 2022년 3분기에는 서울대병원이 7건으로 가장 많은 임상연구를 의뢰했고, 그 중 소아 신증후군 환자 관련 연구가 3건이었다.

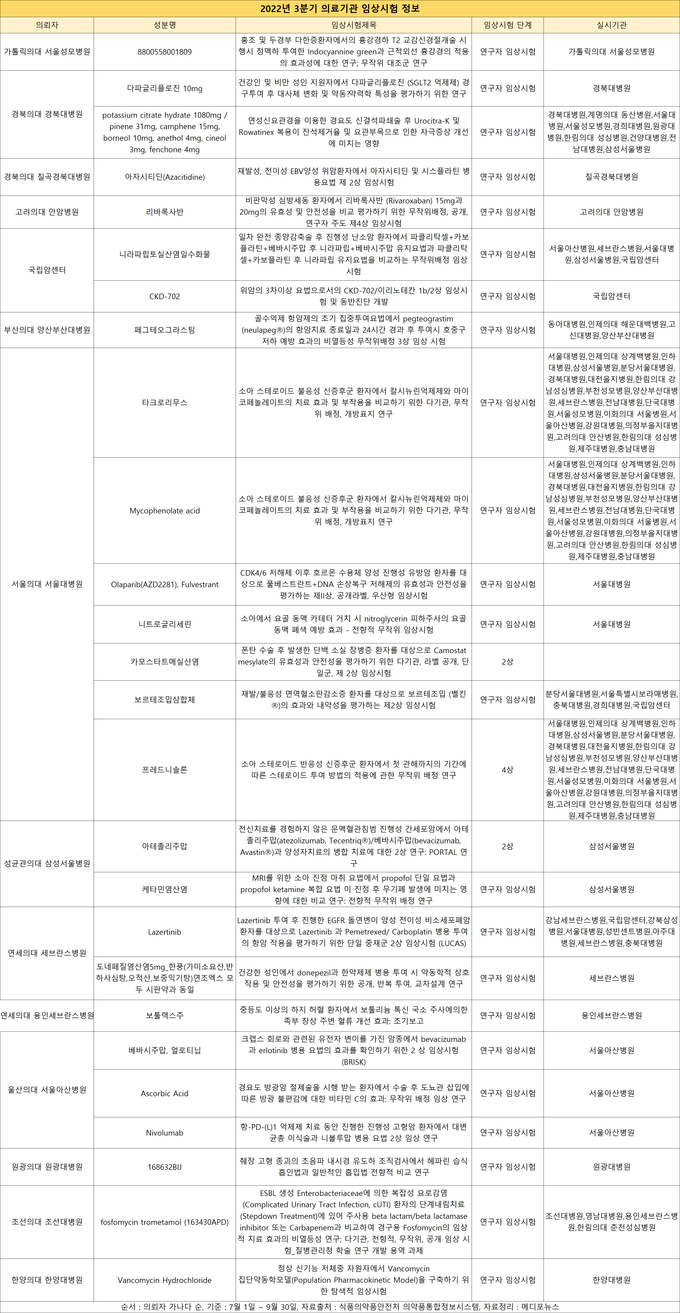
식품의약품안전처 의약품통합정보시스템에 공개된 임상시험 정보에 따르면, 7월 1일부터 9월 30일까지 승인된 전체 26개의 임상시험 중 서울대병원이 7건(성분명 ▲타크로리무스, ▲Mycophenolate acid, ▲Olaparib(AZD2281), ▲Fulvestrant, ▲니트로글리세린, ▲카모스타트메실산염, ▲보르테조밉삼합체, ▲프레드니솔론)으로 가장 많은 임상연구를 의뢰했다.
이중 ▲타크로리무스와 ▲Mycophenolate acid, ▲프레드니슬론을 다룬 연구가 소아 신증후군 환자와 관련된 다기관-무작위 배정 연구로서 22개 의료기관이 참여한 임상시험으로 진행됐다.
각각 소아 스테로이드 불응성 신증후군 환자에서 칼시뉴린억제제와 마이코페놀레이트의 치료 효과 및 부작용을 비교하고(타크로리무스와 Mycophenolate acid), 소아 스테로이드 반응성 신증후군 환자에서 첫 관해까지의 기간에 따른 스테로이드 투여 방법의 적용에 관한 연구(프레드니슬론)였다. 프레드니슬론 연구는 4상 임상시험이 진행되고 있다.
다음으로 많은 임상연구를 의뢰한 의료기관은 서울아산병원으로, ▲베바시주맙, 얼로티닙, ▲Ascorbic Acid, ▲Nivolumab에 관련된 3건의 연구를 의뢰했다.
경북대병원, 국립암센터, 삼성서울병원, 세브란스병원도 3분기에 각 2건씩 임상연구를 의뢰했다.
현재 연구자 임상시험 외 2상 임상시험이 진행되고 있는 연구는 2건으로 서울대병원의 ▲카모스타트메실산염과 삼성서울병원의 ▲아테졸리주맙 연구였다.
2022년 3분기에 진행된 의료기관 임상시험 정보에 관한 자세한 내용은 아래 표에서 확인할 수 있다. 순서는 병원 이름 가나다 순이다.

이형규 기자 kyu7179@medifonews.com
< 저작권자 © Medifonews , 무단전재 및 재배포금지 >
- 본 기사내용의 모든 저작권은 메디포뉴스에 있습니다.
