에자이 ‘렌비마’, 갑상선암∙신장암 이어 간암 정복 나서
갑상선암에 NICE 권고 획득, 간암학회 가이드라인 개정 예고 등 청신호
- 김윤미 기자 kym@medifonews.com
- 등록 2018-02-19 05:30:00
 에자이의 표적항암제 ‘렌비마(성분명 렌바티닙)’가 최근 10여 년간 간암 분야의 표준치료제로 사용되어 온 ‘넥사바(성분명 소라페닙)’와의 비교 임상에서 비열등성을 입증했으며, 무진행생존기간(PFS), 질병진행까지 걸린 시간(TTP), 객관적 반응률(ORR) 등에서 우수한 효과를 보이며, 2018년 간암 치료제로의 입성을 확실시했다.
에자이의 표적항암제 ‘렌비마(성분명 렌바티닙)’가 최근 10여 년간 간암 분야의 표준치료제로 사용되어 온 ‘넥사바(성분명 소라페닙)’와의 비교 임상에서 비열등성을 입증했으며, 무진행생존기간(PFS), 질병진행까지 걸린 시간(TTP), 객관적 반응률(ORR) 등에서 우수한 효과를 보이며, 2018년 간암 치료제로의 입성을 확실시했다.
뿐만 아니라 최근 영국 NICE (The National Institute for Health and Care Excellence)가 갑상선암 치료에 '렌비마' 사용 권고를 최종 결정하며, 수술이나 방사선요법 후 전이된 갑상선암 치료에서 '렌비마'의 급여 사용이 가능해졌다. 이는 유럽(EMA)에서 '렌비마'가 승인된 지 3년 만에 일이다.
에자이는 지난 16일 영국 NICE가 방사성요오드에 불응한 성인의 진행성, 국소 진행성 또는 전이성 분화 갑상선암 치료제로 ‘렌비마’의 사용 권고를 최종 결정했다고 전했다. 참고로 '렌비마'는 지난 2015년 5월 유럽에서 해당 적응증으로 승인 받았으며 6월 영국에서 출시된 바 있다.
'렌비마'는 방사성요오드에 불응한 갑상선암 환자에서 위약과 비교해 무진행생존기간(PFS)을 14.7개월까지 유의하게 향상시키는 것으로 나타나, 2018년 1월에는 미국 FDA으로부터 혁신치료제 지정(The Breakthrough Therapy Designation)을 받았다.
또한 ‘렌비마’는 2016년 9월에는 혈관내피 성장인자(VEGF) 표적치료 경험이 있는 진행성 신세포암 성인 환자에서 ‘아피니토(성분명 에베로리무스)'와 병용요법으로 허가를 취득했다(상품명 ‘키스플릭스', 'Kisplyx’).
여기에 더해 영국 NICE 지난 2017년 12월 ‘렌바티닙’과 ‘에베로리무스’ 병용요법을 이전에 VEGF 표적 치료를 한 성인의 진행성 신장암 치료 옵션으로 추천하며 호재에 호재를 더했다.
에자이는 지난 2일 발표한 2017년 3분기 보고서를 통해 2018년도 ‘렌비마’의 청사진을 전했다.
미국에서의 갑상선암 1차 치료제로의 사용, 유럽에서의 NICE 신장암 치료옵션으로의 권고 등을 언급하며, 미국과 유럽 등지에서 2가지 적응증으로 크게 성장하고 있다고 말했다.
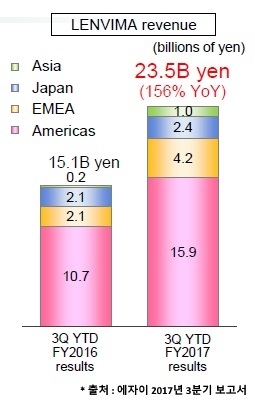 에자이는 미국, 유럽, 일본, 아시아에서의 ‘렌비마’ 수익을 발표하며, 2017년 3분기 수익이 전년 동기 대비 156% 성장한 235억 엔(약 2,364억 원)에 달한다고 전했다.
에자이는 미국, 유럽, 일본, 아시아에서의 ‘렌비마’ 수익을 발표하며, 2017년 3분기 수익이 전년 동기 대비 156% 성장한 235억 엔(약 2,364억 원)에 달한다고 전했다.
뿐만 아니라 에자이는 미국, 유럽, 호주, 캐나다, 중국, 일본, 대만 등지에서 이미 ‘렌비마’의 간암 치료제로의 승인 심사를 요청한 상태로, 올해 상반기 내 미 FDA 승인을 기대하고 있다고 밝혔다.
에자이는 REFLECT 연구를 통해 간암에서의 ‘렌비마’ 효능과 안전성을 입증했다.
REFLECT 연구는 10여 년간 간암 표준치료제로 사용되어 온 ‘소라페닙’과의 비교 임상을 통해 ‘렌비마’의 비열등성을 입증하기 위한 다기관 오픈라벨, 무작위, 글로벌 3상 임상연구로, 그 결과는 지난 9일 란셋(Lancet) 온라인판에 게재된 바 있다.
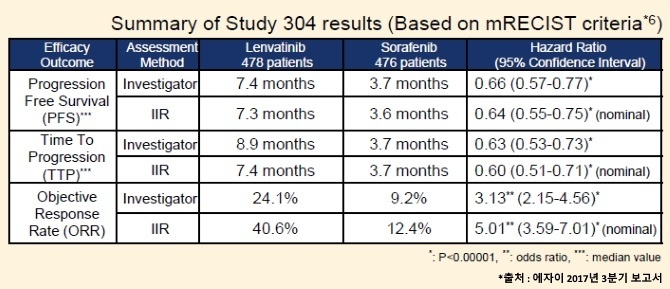
‘절제 불가능한 간세포암 환자의 1차 치료에서의 렌바티닙과 소라페닙의 비교: 무작위 3상 비열 등성 시험’이란 제목으로 발표된 연구 결과에 따르면, 렌바티닙 투여군의 생존기간(중앙값)은 13.6개월, 소라페닙 투여군은 12.3개월로 비열등성을 입증했다.
뿐만 아니라 에자이가 발표한 바에 따르면, 무진행생존기간(PFS), 질병진행까지 걸린 시간(TTP), 객관적 반응률(ORR)에서는 렌바티닙 투여군이 소라페닙 투여군과 비교해 유의하게 우월한 결과를 나타내며 그 효과를 입증했다고 전했다.
이밖에도 신장암이나 자궁내막암, 간암에서의 항 PD-1 면역항암제와의 병용요법으로 여러 임상이 진행 중에 있고, 현재까지 긍정적인 결과를 보이고 있어 향후 ‘렌비마’의 성장에는 청신호가 켜질 전망이다.
 한편, 국내에서도 ‘렌비마’의 간암 치료제로의 입성이 준비 중에 있다. 대한간암학회는 지난 정기 학술대회에서 간암 치료 분야에 새로운 약제들의 등장을 주목하며, 간암 치료 가이드라인의 개정 필요성을 언급한 바 있다.
한편, 국내에서도 ‘렌비마’의 간암 치료제로의 입성이 준비 중에 있다. 대한간암학회는 지난 정기 학술대회에서 간암 치료 분야에 새로운 약제들의 등장을 주목하며, 간암 치료 가이드라인의 개정 필요성을 언급한 바 있다.
현장에서 예상한 가이드라인은 1차 치료제로 소라페닙과 렌바티닙, 2차 치료제로는 ‘레고라페닙’과 ‘카보잔티닙’ 그리고 면역항암제 ‘니볼루맙’이 언급됐으며, 대한간암학회는 6월 가이드라인 개정을 통한 새로운 간암 치료약제의 반영을 예고했다.
- [동정]암젠, 아동·청소년 생명과학 교육 캠페인 서울시장 표창 수상
- [동정]칠곡경북대병원 성인 수두증 클리닉, 30억원 치매극복 기술개발 과제 수주
- [동정]갑상선 수술 관련 비디오 후두경 통한 기관삽관 유용성 입증
- [동정]한국머크 바이오파마, ‘일∙가정 양립 우수 기업’ 선정
- [동정]고대 구로병원 송준영 교수, 질병청·국립보건연구원 학술연구용역 과제 선정
- [동정]일동후디스 하이뮨, 브랜드파워 단백질보충제 부문 2년 연속 1위
- [동정]서울성모병원 정미향 교수, 국제학술지 유럽예방심장학회지 부편집장 임명
- [동정]한올바이오파마, 국가산업대상 ‘연구개발’ 부문 수상
- [동정]제주대병원 연구팀, 국제학술지에 심장재활 논문 게재
- [동정]동화약품, 박진 신임 공장장 취임















